Введение. Несмотря на существование различных методов лечения больных локализованным раком предстательной железы (РПЖ), «золотым» стандартом все еще остается радикальная простатэктомия (РПЭ). Это связано с тем, что операция обеспечивает полноценное удаление пораженного злокачественной опухолью органа, лучший контроль возможного рецидива, более точное определение стадии заболевания, а также наиболее благоприятные отдаленные онкологические результаты и относительно высокое качество жизни пациентов [1–3]. В то же время РПЭ является технически сложным оперативным вмешательством и сопряжена с высоким риском возникновения осложнений, одним из которых считается стрессовое недержание мочи. Недержание мочи различной степени возникает достаточно часто после РПЭ. При этом необходимо указать, что даже при большом хирургическом опыте существенно снизить частоту данного осложнения не удается. Так, по данным крупнейших исследований последних лет, включивших от 524 до 4265 пациентов и имевших медиану наблюдения 12 и более месяцев, недержание мочи встречалось у 6–41,9% больных [4–7]. Внимание к исследуемой проблеме обусловлено тем, что возникновение недержания мочи крайне негативно отражается на качестве жизни больных РПЖ в послеоперационном периоде, ограничивая их физическую и социальную активность, что зачастую служит причиной неудовлетворенности пациента перенесенной операцией и возникновения страха перед радикальным лечением из-за возможного наступления этого осложнения. В связи с этим выявление объективных, не связанных с техническим прогнозированием факторов риска развития недержания мочи после РПЭ, представляется актуальной задачей, направленной на снижение вероятности появления этого осложнения. Исходя из вышеперечисленных обстоятельств, и было проведено настоящее исследование.
 Материалы и методы. В исследование включены 180 больных РПЖ в возрасте от 48 до 74 лет (медиана – 63 года), которым на базе городской клинической больницы им. С.П. Боткина Москвы с 2011 по 2013 г. была выполнена открытая позадилонная РПЭ. Нервосберегающая методика операции применена к 34 (18,9%) больным, при этом сосудисто-нервные пучки сохранены с двух сторон у 19 пациентов и с одной – у 15. В исследование не включали пациентов с наличием в анамнезе неоадъювантного лечения РПЖ и оперативных вмешательств по поводу травм и заболеваний органов малого таза и половой системы.
Материалы и методы. В исследование включены 180 больных РПЖ в возрасте от 48 до 74 лет (медиана – 63 года), которым на базе городской клинической больницы им. С.П. Боткина Москвы с 2011 по 2013 г. была выполнена открытая позадилонная РПЭ. Нервосберегающая методика операции применена к 34 (18,9%) больным, при этом сосудисто-нервные пучки сохранены с двух сторон у 19 пациентов и с одной – у 15. В исследование не включали пациентов с наличием в анамнезе неоадъювантного лечения РПЖ и оперативных вмешательств по поводу травм и заболеваний органов малого таза и половой системы.
По данным предоперационного обследования, индекс массы тела (ИМТ) пациентов варьировался от 20,6 до 39,4 (медиана – 28,2), уровень простатического специфического антигена (ПСА) – от 4,6 до 39,8 нг/мл (медиана – 8,9 нг/мл), объем предстательной железы – от 20 до 145 см3 (медиана – 46 см3).
В зависимости от результатов послеоперационного морфологического исследования структура больных РПЖ имела следующие характеристики:
1) стадия:
- pT2 – 133 больных (73,9%),
- pТ3a – 36 больных (20%),
- pТ3b – 11 больных (6,1%);
2) сумма баллов по Глисону:
- ≤ 6 баллов – 48 больных (26,7%),
- 7 баллов – 121 больной (67,2%),
- ≥ 8 баллов – 11 больных (6,1%);
3) статус хирургического края:
- отрицательный край – 170 (94,4%) больных,
- положительный край – 10 (5,6%) больных.
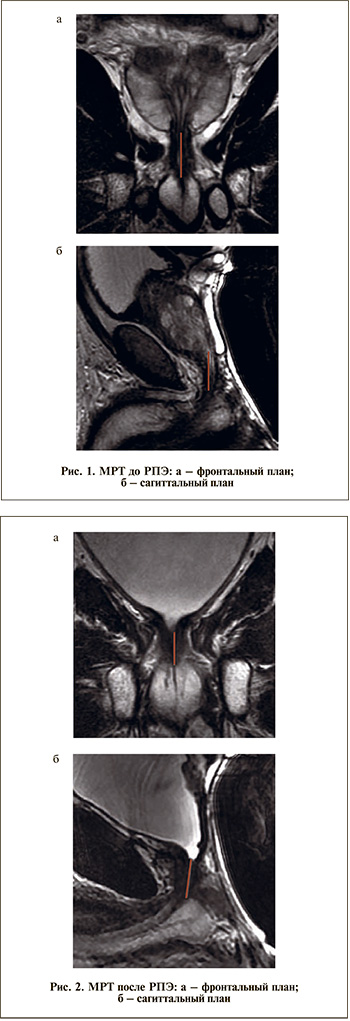
Всем пациентам до и после РПЭ выполняли магнитно-резонансную томографию (МРТ) для определения длины мембранозного отдела уретры и формы апекса предстательной железы. Измерения длины мембранозного отдела уретры производили во фронтальной и сагиттальной плоскостях (рис. 1, 2). МРТ проводили в Центре лучевой диагностики ФГБУ «Лечебно-реабилитационный центр» Минздрава России на аппарате «Discovery MR750» (General Electric, USA) с напряженностью магнитного поля 3 Тл.
Сроки послеоперационного наблюдения пациентов составляли от 3 до 18 месяцев (медиана – 9 месяцев). Степень стрессовой формы недержания мочи после РПЭ определяли по частоте используемых прокладок (pad-тест) согласно следующей градации: 1-я степень – полное удержание мочи; 2-я степень – 1 прокладка в день; 3-я степень – 2–3 прокладки в день; 4-я степень – 3–4 прокладки в день; 5-я степень – тотальное недержание мочи.
Статистическая обработка данных проводилась с использованием пакета прикладных программ «Statistica v.17.0» (StatSoft, USA). Сравнение групп больных по частоте недержания мочи в зависимости от различных параметров обследования проводили с помощью U-критерия Манна–Уитни. Достоверными считали различие между группами по какому-либо признаку при значениях p<0,05. Для определения вклада исследуемых пред- и послеоперационных показателей в вероятность возникновения недержания мочи после РПЭ выполнили многофакторный регрессионный логистический анализ с определением относительного риска (ОР) и 95% доверительного интервала (ДИ) всех признаков.
Результаты исследования и их обсуждение. Пока-затели функции удержания мочи при медиане наблюдения после операции 9 месяцев имели следующие значения. Полное удержание мочи наблюдали у 166 (92,2%) больных, необходимость использования 1 прокладки в день – у 6 (3,3%) больных, 2–3 прокладок – у 5 (2,8%) больных, 4 и более прокладок – у 2 (1,1%) больных, тотальное недержание мочи – у 1 (0,6%) больного. Таким образом, частота недержания мочи различной степени составила 7,8% (14 больных). Состояние функции удержания мочи в зависимости от различных пред- и послеоперационных параметров продемонстрировано в табл. 1.
По данным МРТ было выявлено, что показатели предоперационной длины мембранозного отдела уретры варьировались от 6 мм до 24 мм (медиана – 14 мм), послеоперационной длины – от 4 до 21 мм (медиана – 13 мм). Выявлены следующие особенности зависимости функции удержания мочи после РПЭ от длины мембранозного отдела уретры: при предоперационной его длине > 14 мм мочу удерживали в 79% случаев, а при ≥ 14 мм – в 51% (p<0,05). При послеоперационной длине мембранозного отдела уретры >13 мм мочу удерживали в 87% случаев, а при ≤13 мм – 41% (p<0,05).
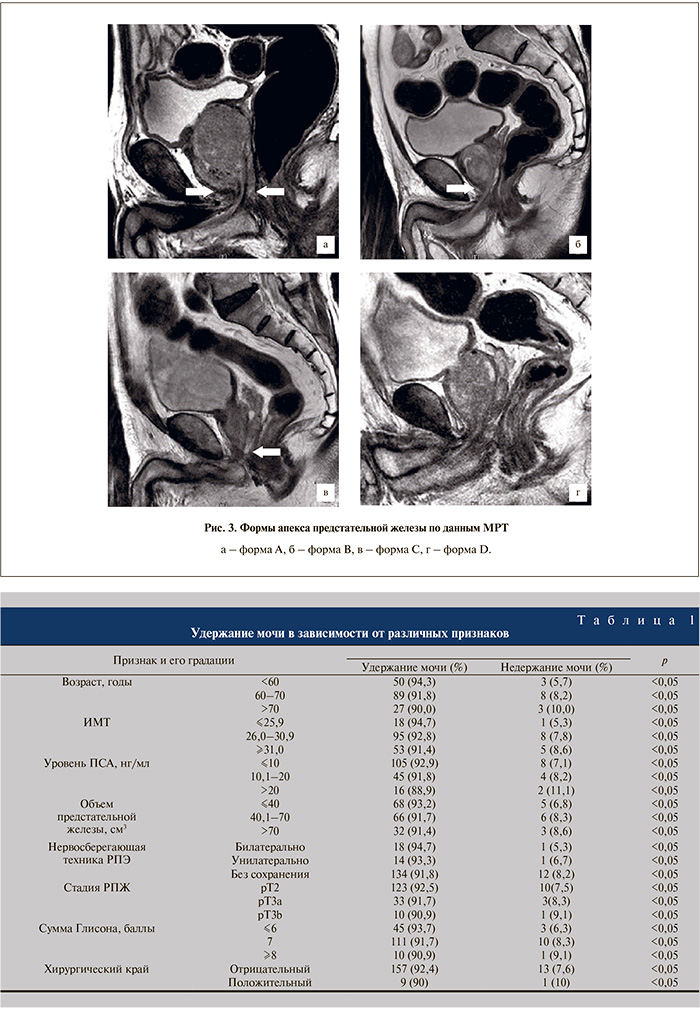
Форму апекса предстательной железы определяли путем оценки соотношения апекса и наружного сфинктера при сагиттальном срезе МРТ на основании классификации S.E. Lee и соавт. [8]. Было выявлено, что в данной когорте пациентов апекс предстательной железы покрывал сфинктер уретры циркулярно (форма апекса А) в 65 (36,1%) наблюдениях, спереди (форма B) – в 41 (22,8%), сзади (форма C) – в 47 (26,1%), не покрывал вообще (форма D) – в 27 (15%) (рис. 3).

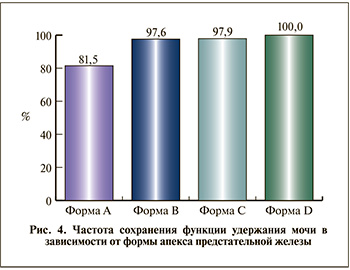
Оказалось, что функция удержания мочи после РПЭ существенно зависит от формы апекса предстательной железы (рис. 4). Наибольшую частоту недержания мочи регистрировали при форме А. Видимо, максимальный риск повреждения сфинктера в процессе отделения предстательной железы от уретры обусловлен тем, что при данной форме сфинктер уретры со всех сторон покрыт апексом предстательной железы.
Многофакторный логистический регрессионный анализ показал, что из всех изучаемых признаков достоверное влияние на риск возникновения недержания мочи после РПЭ оказывают длина мембранозного отдела уретры, форма апекса предстательной железы и возраст больных (табл. 2).
 Из таблицы видно, что при рассмотрении влияния возраста на ОР развития недержания достоверная разница существует только между пациентами в возрасте старше 70 и моложе 60 лет. Вероятно, возрастные инволюционные нейротрофические изменения в зоне сфинктерного аппарата существенно усугубляются операционной травмой, что приводит к большей частоте проявлений недержания мочи у мужчин старшей возрастной группы. Аналогичная закономерность была прослежена в исследовании T. Schlomm и соавт. [9], которые отметили разницу между указанными возрастными группами по риску возникновения недержания со значением p=0,0412 (т.е. p<0,05). Так как авторы в своей работе руководствовались критерием достоверности p<0,001, указанная разница по возрасту ими была признана статистически незначимой. Однако следует добавить, что в другом крупном исследовании возраст не был отнесен к независимым предикторам недержания мочи после РПЭ [10].
Из таблицы видно, что при рассмотрении влияния возраста на ОР развития недержания достоверная разница существует только между пациентами в возрасте старше 70 и моложе 60 лет. Вероятно, возрастные инволюционные нейротрофические изменения в зоне сфинктерного аппарата существенно усугубляются операционной травмой, что приводит к большей частоте проявлений недержания мочи у мужчин старшей возрастной группы. Аналогичная закономерность была прослежена в исследовании T. Schlomm и соавт. [9], которые отметили разницу между указанными возрастными группами по риску возникновения недержания со значением p=0,0412 (т.е. p<0,05). Так как авторы в своей работе руководствовались критерием достоверности p<0,001, указанная разница по возрасту ими была признана статистически незначимой. Однако следует добавить, что в другом крупном исследовании возраст не был отнесен к независимым предикторам недержания мочи после РПЭ [10].
Данные о длине мембранозного отдела уретры и форме апекса предстательной железы, получаемые в ходе МРТ, являются ценной информацией, позволяющей еще в предоперационном периоде детально спланировать ход хирургических манипуляций во время оперативного вмешательства. Важность учета этих параметров при выполнении РПЭ отмечены в ряде последних работ [8, 9].
Что касается других факторов, потенциально играющих роль предикторов инконтиненции после РПЭ, то по этому поводу в литературе существуют противоречивые данные [11–15]. И наши исследования также не обнаружили их значимого влияния на возникновение недержания мочи.
Заключение. Настоящее исследование показало, что использование на предоперационном этапе МРТ позволяет выявлять индивидуальные особенности соотношения апекса предстательной железы и сфинктера уретры и, следовательно, попытаться сохранить максимальную длину мембранозного отдела уретры в ходе позадилонной РПЭ. Прецизионная техника простатэктомии наряду с подбором пациентов по возрастному признаку существенно снижают вероятность возникновения стрессового недержания мочи после оперативного вмешательства.


