Введение. Перкутанная нефролитотрипсия (ПНЛ) остается методом выбора при хирургическом лечении больных с крупными и коралловидными камнями почек [1–5]. Важным этапом ПНЛ, несомненно, остается создание перкутанного доступа в чашечно-лоханочную систему (ЧЛС), который чаще всего выполняется под рентгенологическим контролем. Постоянное использование рентгеноскопии при ча- стых перкутанных вмешательствах на почке может приводить к развитию различных осложнений со стороны медицинского персонала, связанных с длительным воздействием лучей на функцию щитовидной железы, гонад, костного мозга и глаз [6–9]. Самой незащищенной частью тела, подвергающейся постоянному влиянию рентгеновских лучей во время ПНЛ, являются глаза урологов. Поэтому длительная рентгеноскопия во время перкутанных операций может быть причиной развития катаракты [10, 11]. Однако, по данным Международной комиссии по радиационной защите, лимит лучевой нагрузки на глаза оперируемого хирурга заканчивается при выполнении 1200 чрескожных операций на почке в течение одного года, а суммарная доза радиации при этом составляет около 150 мЗв [12]. Согласно результатам проведенных исследований данной комиссии средняя доза радиации при ПНЛ составляет около 0,125 мЗв.
Для снижения риска вышеперечисленных осложнений рентгеноскопии некоторые авторы предлагают выполнять чрескожную нефростомию и нефролитотрипсию под ультразвуковым (УЗ) контролем [13–16]. Подробно описана техника пункционной нефростомии под УЗ-контролем беременных женщин с нарушением уродинамики верхних мочевых путей (ВМП) [17]. В англоязычной литературе встречаются сообщения о ПНЛ под УЗ-контролем больных с одиночными крупными лоханочными камнями почки. Приводим результаты перкутанного удаления камней по данной методике у 68 больных.
Материалы и методы. С 1999 по 2013 г. в клинике урологии Северо-Западного государственного медицинского университета им. И.И. Мечникова ПНЛ выполнена 624 пациентам. В основу данного исследования положены результаты ПНЛ, проведенной 138 (22,1%) больным. Из них мужчин было 74 (53,6%), женщин – 64 (46,4%). Средний возраст больных составил 42,8 года. Пациенты были распределены в две группы. Семидесяти пациентам (1-я группа) операцию выполняли под комбинированным ультразвуковым и рентгенологическим контролем, а 68 (2-я группа) — только под УЗ-контролем. В исследование включили пациентов с крупными лоханочными камнями размером более 2,2 см, требующими создания только одного перкутанного доступа, расширенной ЧЛС, с индексом массы тела менее 28 кг/м² (табл. 1).

Диагноз нефролитиаза установлен на основании жалоб пациента, данных анамнеза и объективного статуса, результатов специальных методов обследования. Кроме ультразвукового, радиоизотопных исследований почек и экскреторной урографии всем больным выполнена спиральная компьютерная томография с 3D-реконструкцией. Вышеперечисленные методы позволили определить размеры и плотность камня, его стереометрическое расположение, изменения морфофункционального состояния почек и ВМП, ангиоархитектонику почки. Функцию почек оценивали на основании данных динамической сцинтиграфии. До операции при наличии воспалительных изменений в анализах мочи проведена антибактериальная терапия.
Все больные оперированы одной бригадой хирургов, на момент исследования имевших опыт выполнения более 400 ПНЛ. Вначале выполняли цистоскопию с катетеризацией мочеточника. Под контролем эндоскопа катетер 6 или 7 Ch устанавливали максимально высоко, чтобы его дистальный конец располагался в лоханке или верхней чашке. Во время катетеризации мочеточника рентгеноскопию не проводили, а индикатором адекватной локализации катетера в ЧЛС было активное выделение по нему мочи. При достаточном расширении ЧЛС пункцию и дилатацию свища можно проводить без предварительной катетеризации мочеточника. Однако ретроградно установленный катетер позволяет путем введения стерильного раствора сравнительно расширить ЧЛС перед ее пункцией. Кроме того, он является хорошим ориентиром при выполнении нефроскопии, исключает миграцию мелких осколков в мочеточник, снижает травму пиелоуретерального сегмента щипцами. После катетеризации мочеточника эндо- скоп извлекали, в мочевой пузырь устанавливали катетер Фолея. Далее больного переворачивали на живот, производили УЗИ оперируемой почки, определяли оптимальную для пункции ЧЛС точку. С помощью УЗ-сканера измеряли расстояние от этой точки на коже до полостной системы почки. Данное расстояние в дальнейшем использовали для определения глубины проведения бужа до ЧЛС во время дилатации пункционного свища. По мочеточниковому катетеру вводили стерильный физиологический раствор, что позволяло сравнительно расширить ЧЛС перед пункцией. Затем под УЗ-контролем с использованием ультразвуковой насадки пунктировали ЧЛС через среднюю или нижнюю чашку. В большинстве случаев пункцию осуществляли под XII ребром, и только 6 пациентам с камнем левой почки она выполнена в двенадцатом межреберье. Активное выделение ретроградно вводимой жидкости с индигокармином по игле указывало на ее адекватное нахождение в ЧЛС. При пункции ЧЛС немаловажен момент проведения иглы через чашку в лоханку, что облегчает последующую установку струны. Далее под УЗ-контролем по игле устанавливали сверхжесткий проводник. Дилатацию пункционного доступа осуществляли бужами Amplatz. При этом глубина бужирования не превышала предварительно установленного расстояния от кожи до полостной системы почки. При расширении пункционного канала последовательно использовали только несколько бужей (обычно 16, 22, 26 или 28 Ch), и каждый дилататор проводили под УЗ-контролем. Однако урологам с небольшим опытом перкутанных вмешательств на почке рекомендуем выполнять пошаговое бужирование пункционного доступа. После установки кожуха Amplatz жесткую струну не извлекали, и она оставалась в качестве страховочного проводника. Осмотр ЧЛС производили жестким нефроскопом 24 Ch, для дезинтеграции камня использовали ультразвуковой литотриптер. В конце операции для исключения резидуальных камней ЧЛС выполняли УЗИ почки. Затем под контролем нефроскопа дистальный конец кожуха Amplatz устанавливали глубже в лоханку. Эндоскоп извлекали, по кожуху проводили баллонный катетер, раздували его баллон. Только после этого удаляли кожух, что обеспечивало адекватную установку нефростомиче- ского дренажа и надежное дренирование ЧЛС почки. Нефростому фиксировали к коже, больного переворачивали на спину. В послеоперационном периоде проводили антибактериальную и инфузионную терапию. Уретральный и мочеточниковый катетеры удаляли на следующий день после операции. На 2-е или 3-и сутки выполняли обзорную рентгенографию мочевых путей и антеградную пиелоуретерографию. В отсутствие резидуальных камней и адекватной проходимости мочеточника нефростомический дренаж удаляли и выписывали больного на амбулаторное лечение.
В ходе сравнительного анализа оценивали операционное время, объем кровопотери, сроки госпитализации, количество интра- и послеоперационных осложнений.
Результаты. Перкутанный доступ был успешно выполнен всем 138 больным. Послеоперационные осложнения (обострение хронического пиелонефрита, макрогематурия), купированные консервативным путем, наблюдали у 14,3% больных 1-й группы и у 14,7% – 2-й.
Результаты исследования показали, что группы статистически значимо не различались по эффективности операции, объему кровопотери, срокам госпитализации (табл. 2). Кровотечения, требующего переливания крови, и травм соседних органов не было. Эффективность ПНЛ для больных 1-й группы составила 95,7 %. К дополнительным вмешательствам (дистанционная литотрипсия) прибегли в 3 (4,3 %) случаях. Во 2-й группе у 64 (94,1 %) больных камень был полностью удален и 4 (5,9%) больным по поводу резидуальных камней выполнена дистанционная литотрипсия. По данным динамической сцинтиграфии у всех пациентов отмечена нормализация уродинамики ВМП и улучшение функции почки.
Приводим клиническое наблюдение успешной ПНЛ камня под УЗ-контролем.
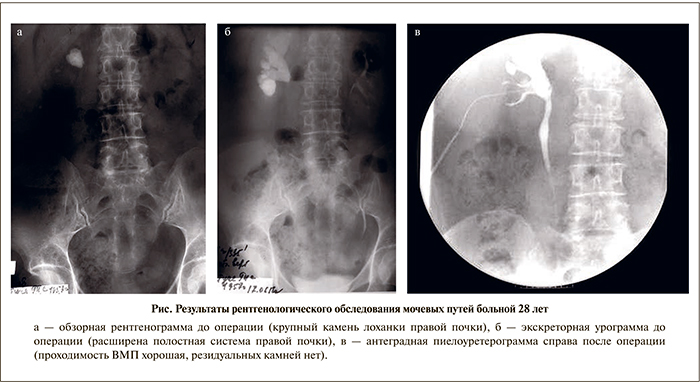
Б о л ь н а я 36 лет госпитализирована в нашу клинику 15.10.13 с жалобами на боли в правой поясничной области. По данным УЗИ и экскреторной урографии выявлены крупный камень лоханки правой почки, расширение ее полостной системы (см. рис. а, б). С учетом больших размеров камня локализацию его в лоханке и расширение ЧЛС решено выполнить ПНЛ справа под УЗ-контролем. После катетеризации мочеточника в положении на животе под УЗ-контролем произведена пункция ЧЛС через нижнюю чашку. По струне пункционный канал бужирован до 28 Ch, установлен кожух Amplatz. При нефроскопии визуализировался крупный камень лоханки. Выполнена контактная литотрипсия, крупные осколки извлечены. При контрольном УЗИ почки резидуальных камней нет. Интра- и послеоперационных осложнений не было.
На 2-е сутки выполнены обзорная рентгенография мочевых путей и антеградная пиелоуретерограмма справа (см. рис. в): резидуальных камней в проекции мочевых путей нет, проходимость ВМП хорошая. Нефростомический дренаж извлечен, больная выписана на амбулаторное лечение.
В данном клиническом случае ПНЛ под УЗ-контролем позволила полностью удалить крупный камень лоханки без использования рентгено- скопии.

Обсуждение. Правильная пункция ЧЛС и формирование перкутанного доступа – важные факторы достижения хороших результатов при ПНЛ. Частое использование рентгеноскопии при создании перкутанного доступа может быть причиной развития различных осложнений со стороны медицинского персонала, связанных с воздействием лучей на функцию щитовидной железы, гонад, костного мозга и глаз. Кроме того, J. Loree и соавт. [18] в эксперименте установили, что продолжительная флюороскопия индуцирует различные молекулярные изменения в тканях животных, в том числе и канцерогенные. В связи с этим при создании пункционного доступа во время ПНЛ необходим альтернативный контроль, позволяющий минимизировать использование рентгеноскопии.
За последние годы в литературе появились работы о возможности выполнения ПНЛ под УЗ-контролем. A. Basiri и соавт. [19] сообщают о 94%-ном успехе при пункции полостной системы почки под УЗ-контролем. При этом у трети оперированных пациентов расширение ЧЛС было недостаточным для адекватной пункции. Другим фактором, увеличивающим успех пункции до 100%, было ретроградное введение стерильного раствора через установленный катетер, значимо расширяющий ЧЛС и облегчающий ее пункцию. Подобную методику использовали M. Etemadian и соавт. [20], которые указывают, что для адекватной пункции чашки необходимо использовать УЗ-сканер с пункционной насадкой. M. Desai и соавт. [16] свидетельствовали: перкутанный доступ под ультразвуковым контролем хорошо выполнять с насадкой для иглы, так как пункционная линия адекватно наводится на нужную чашку и на мониторе хорошо виден момент пункции. По мнению [14, 16], доступ в ЧЛС должен осуществляться опытным урологом. W. Gamal и соавт. [13] сообщили о 2 (5,3%) эпизодах перфорации ЧЛС при дилатации свища металлическими бужами, так как на мониторе сложно контролировать прохождение бужа. Поэтому они рекомендуют применять тефлоновые бужи Amplatz, при использовании которых перфорации ЧЛС не было. В работе [15] перфорация ЧЛC при бужировании тефлоновыми дилататорами возникла в 4 (8,5%) случаях, несмотря на то что были оперированы больные с одиночными камнями лоханки, как и в серии пациентов W. Gamal и соавт. [13]. Однако у пациентов этой группы диаметр камней был больше (24–46 мм), а по данным УЗИ почки имела место выраженная дилатация лоханки и чашечки расширены незначительно. У X. Zou и соавт. [20], прооперировавших 92 больных, необходимость в повторной пункции возникла для 22,8% больных, что выше показателей, полученных W. Gamal и соавт. [13]. Однако большинство (75%) больных этой группы имели множественные и коралловидные камни. W. Gamal и соавт. [13] второй доступ использовали только в отношении 2 (5,8%) больных. В ходе выполнения ПНЛ рентгеновская дуга всегда была в наличии в операционной, но потребности в ней не возникало. Однако в другой серии УЗ контролируемой ПНЛ рентгенологический контроль понадобился 2 из 47 больных [10].
W. Gamal и соавт. [13] успешно выполнили ПНЛ под УЗ-контролем 8 больным с рентгеннегативными камнями. Этот факт указывает на преимущества и результаты УЗ-контролируемой ПНЛ при рентгеннегативных камнях, о чем также сообщали M. Hosseini и соавт. [15]. При рентгеннегативных камнях ПНЛ под рентгенологическим контролем особого преимущества не имеет, так как не можем контролировать дробление камня и наличие осколков на рентгене, камень видим только как дефект наполнения. А на УЗИ хорошо видны резидуальные камни. К повторным ПНЛ W. Gamal и соавт. [13] прибегали в отношении 6% больных, а M. Hosseini и соавт. [15] – 6,4%. Однако размеры камней у оперированных ими больных были сравнительно больше. M. Osman и соавт. [14] сообщили о необходимости дополнительных процедур (дистанционная литотрипсия, повторные ПНЛ, уретероскопия) после первичной ПНЛ у 33% больных, так как большинство из них страдали коралловидными камням. В нашей группе ПНЛ выполнена по поводу одиночных крупных камней лоханки, поэтому дистанционная литотрипсия потребовалась только 4 (5,9%) больным. А. Basiri и соавт. [18] констатировали небольшое количество интра- и послеоперационных осложнений: лишь у 5 пациентов возникло показание к проведению гемотрансфузии, и все они имели коралловидные камни. Количество осложнений ПНЛ, выполненных под УЗ-контролем, зарегистрированных у больных, оперированных W. Gamal и соавт. [13] и нами, было минимальным, так как размеры камней были меньше (менее 30 мм).
Таким образом, ПНЛ, проводимая под УЗ-контролем, имеет такие преимущества, как высокая частота успешных пункций ЧЛС, возможность интраоперационного обнаружения и мониторирования рентгенопозитивных и рентгеннегативных камней, отсутствие рентгеновской нагрузки и возможность визуализации находящихся в зоне пункции органов. К факторам, определяющим успех подобных операций, можно отнести размер камня менее 30 мм, достаточное расширение ЧЛС, локализацию камня в лоханке, использование пункционной насадки и опыт хирурга. В связи с этим небольшой опыт хирурга, наличие множественных и коралловидных камней считаем основанием для отказа от выполнения ПНЛ под ультразвуковым контролем.
Заключение. Перкутанная нефролитотрипсия под УЗ-контролем больных с крупными одиночными камнями лоханки и расширенной ЧЛС считается эффективным методом лечения. Она позволяет выполнять ПНЛ без использования рентгеноскопии и снижать объем лучевой нагрузки на оперирующего уролога.



