На протяжении многих лет простатспецифический антиген (ПСА) сыворотки крови остается самым часто используемым маркером в диагностике и стадировании, а также послеоперационном мониторинге состояния пациентов, перенесших операцию по поводу рака предстательной железы (РПЖ). Вместе с тем данная методика не совершенна ввиду наличия ложноотрицательных результатов, неопределенных рамок референсных значений и отсутствия возможности достоверной оценки эффективности проведенного лечения. У пациентов с уровнем общего ПСА от 4 до 10 нг/мл РПЖ диагностируется только в каждом четвертом случае, а частота негативных биопсий может достигать 80% [1]. Поскольку ПСА не является раковоспецифическим маркером, повышение его уровня может происходить как при наличии РПЖ, так и в случае доброкачественной гиперплазии предстательной железы (ДГПЖ), острой задержки мочи, инфекций и/или воспалительного процесса, а также после различных манипуляций (массаж предстательной железы, пальцевое ректальное исследование [ПРИ], биопсия предстательной железы) в результате нарушения проницаемости тканевых барьеров и в ходе оперативных вмешательств на предстательной железе (радикальная простатэктомия [РПЭ], трансуретральная резекция, криоаблация и др.), сопровождаемых повреждением базальных клеток, разрушением базальной мембраны и как следствие – выходом эндогенного ПСА в кровь [2].
В настоящее время в клинической практике используется несколько форм ПСА, каждой из которых отводят определенную роль в диагностике РПЖ: общий ПСА (оПСА), свободный ПСА (свПСА), связанный ПСА (cПСА). С целью повышения диагностической ценности оПСА, особенно в случае поиска ранних форм РПЖ, используется ряд индексов: отношение свПСА/оПСА (%свПСА), плотность ПСА (ПСАD), скорость прироста ПСА (ПСАV), уровень оПСА с учетом возраста и др. [3, 4]. Значительный прогресс в молекулярной биологии, генетике и нанотехнологии позволил внедрить в клиническую практику новые маркеры РПЖ, из которых наиболее перспективными и изученными являются [-2]проПСА, РСА3 и индекс здоровья простаты (PHI). Несмотря на это, вопросы гипердиагностики клинически незначимого РПЖ и позднего выявления агрессивных форм по-прежнему остаются главной проблемой онкоурологии.
К концу 2016 г. разработана масса более точных маркеров, которые среди прочих включают 4Кscore, тест TMPRSS2-ERG, SChLAP1, SelectMDx, ConfirmMDx и ELAVL1. Перспективу внедрения новых маркеров в клиническую практику и возможность замены ПСА еще предстоит оценить, однако уже сейчас можно отметить, что данные маркеры могут быть актуальными при определении необходимости проведения первичной или повторной биопсии предстательной железы, а также при определении метастазирования и биохимического рецидива РПЖ.
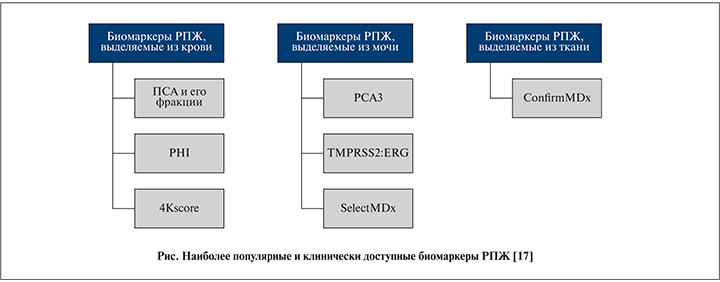
Активное развитие протеомики в совокупности с лабораторной диагностикой привело к обнаружению более 200 потенциальных биомаркеров РПЖ. Каждый маркер РПЖ или тест, создаваемый на основе уже имеющихся маркеров, может быть классифицирован в группу диагностических (скрининговых), прогностических или группу маркеров стратификации. В данной статье приводится описание биомаркеров РПЖ, чья роль в диагностике заболевания была подтверждена проведенными клиническими исследованиями (см. рисунок). Ряд биомаркеров, выделенных из крови, мочи, эякулята или ткани предстательной железы, может быть полезным в принятии решения относительно целесообразности биопсии, снижения частоты ненужных биопсий и выявления клинически значимого рака.
Генетический биомаркер рака простаты РСА3 и тест Progensa
Одним из перспективных методов ранней неинвазивной диагностики РПЖ являются тест-системы, основанные на количественном анализе РНК-продукта гена PCA3, гиперэкспрессия которого наблюдается при малигнизации ткани предстательной железы. В непораженных клетках предстательной железы и клетках доброкачественной гиперплазии ген PCA3 присутствует в минимальных количествах. РНК-продукт гена PCA3 может присутствовать в моче и эякуляте, что предусматривает использование данных биологических жидкостей для неинвазивной диагностики РПЖ [5]. Тест Progensa отражает уровень PCA3, обнаруженного в образцах мочи пациента после ПРИ. Показанием к взятию анализа PCA3 является наличие в анамнезе мужчины (≥50 лет) одной или более биопсии предстательной железы с отрицательным результатом и сохраняющимся подозрением на РПЖ. Значение PCA3<25 свидетельствует о меньшей вероятности обнаружения РПЖ при последующей повторной биопсии простаты.
В то время как многочисленные исследования показывают, что PCA3 с большей точностью позволяет выявлять РПЖ при повторной биопсии по сравнению с оПСА и %свПСА [6, 7], некоторые авторы подчеркивают эффективность PCA3 в диагностике клинически значимого рака при первичной биопсии [8, 9]. Проведя исследование с участием 859 мужчин, J. Wei и соавт. сообщили, что при значении PCA3≤20 пациенты с первичной негативной биопсией могут избежать до 46% повторных биопсий при проценте пропущенных случаев клинически значимого РПЖ не более 3%. Однако при использовании того же порога PCA3 будет пропущено до 13% клинически значимого рака при первичной биопсии [10].
Было показано, что PCA3 не отражает ухудшения общего состояния или наличия осложнений у пациентов, находящихся под активным наблюдением или перенесших РПЭ [11, 12]. Результаты исследования [13] в некоторой степени ограничивают диагностическую ценность PCA3. Выполнив 120 пациентам, подходящим под активное наблюдение, РПЭ, авторы пришли к выводу, согласно которому предоперационное МРТ и определение PHI имели более высокую диагностическую ценность в выявлении клинически значимого рака по сравнению с PCA3. Также установлено, что PHI превосходит PCA3 в прогнозировании клинически значимого РПЖ, в последующем обнаруженного при биопсии и РПЭ [14, 15].
Описанные примеры предопределяют применение PCA3 в сочетании с другими маркерами РПЖ и методами диагностики. Так, например, сочетанное использование PCA3 и мультипараметрической МРТ (мпМРТ), по мнению M. Fenstermaker и соавт. [16], значительно увеличивает частоту выявления клинически значимого РПЖ.
На основе PCA3 было разработано и утверждено несколько номограмм, включая PCPTRC (Prostate Cancer Prevention Trial Risk Calculator). По мнению [17], использование подобной номограммы позволит избегать до 55% ненужных биопсий при доле пропущенных клинически значимых случаев РПЖ, не превышающей 2%.
ПроПСА и PHI
Простатспецифический антиген образуется из неактивного предшественника, который содержит основную последовательность из 7 аминокислот, известную как [-7] проПСА. Активация происходит посредством расщепления его основной последовательности ≥7 аминокислот с помощью калликреинов-2 и -4 с образованием зрелой молекулы ПСА из 237 аминокислот. Частичное расщепление этой основной последовательности приводит к появлению различных изоформ проПСА в зависимости от того, сколько аминокислот остаются связанными с молекулой ПСА. Чаще всего это [-4] проПСА, [-5] проПСА и [-2] проПСА. Было обнаружено, что вариант [-2] проПСА наиболее устойчивый в сыворотке и распространенный среди изоформ проПСА [3, 4].
В 2009 г. D. Makarov и соавт. [18] показали, что анализ крови на [-2] проПСА позволяет определить, у каких пациентов может развиваться агрессивный РПЖ при активном наблюдении, а у каких можно прогнозировать появление так называемой неблагоприятной контрольной биопсии (выявление при контрольной биопсии аденокарциномы ≥7 баллов по Глисону, наличие ≥3 позитивных столбиков или выявление РПЖ в ≥50% ткани любого столбика). На основании данного анализа был разработан индекс здоровья простаты – Prostate Health Index (РHI), математическая формула которого построена на различных соотношениях специфических биомаркеров (оПСА, свПСА и [-2] проПСА). PHI представляется перспективным неинвазивным биомаркером, который может повысить частоту обнаружения РПЖ и предоставить прогностическую информацию относительно имеющегося заболевания.
Многочисленные исследования продемонстрировали высокую эффективность PHI по сравнению с оПСА и свПСА [19–21]. W. Catalona и соавт. [19] опубликовали результаты крупного мультицентрового исследования, в которое были включены 892 пациента, перенесших трансректальную биопсию предстательной железы. У всех пациентов отсутствовали изменения по данным ПРИ, а уровень оПСА был в интервале 2–10 нг/мл. Авторы сделали вывод, согласно которому чувствительность и специфичность PHI (на основании площади ROC-кривых) превышает значения оПСА, свПСА, [-2] проПСА и %свПСА в диагностике клинически значимого РПЖ, а также сопряжено с более высоким баллом по шкале Глисона. Повышение экономической эффективности скрининга с помощью PHI подтверждено в многоцентровом проспективном исследовании, в которое были включены 658 мужчин с уровнем oПСА от 4 до 10 нг/мл [20]. В ходе работы показано, что при пороговом значении PHI 28,6 диагноз РПЖ (сумма Глисона 3+4 и 4+3) будет пропущен лишь в 4,8 и 1,2% случаев. Тем не менее более 30% пациентов с ДГПЖ смогут избежать повторной биопсии предстательной железы, в то время как при использовании оПСА количество данных пациентов не превышает 21,7%.
G. Lughezzani и соавт. [22] разработали номограмму с использованием таких критериев, как возраст, объем предстательной железы, ПРИ, предшествовавшие биопсии в анамнезе, и PHI. По мнению авторов, использование данной номограммы превосходит базовое исследование с использованием только лишь одного оПСА и позволяет эффективнее прогнозировать клинически значимый рак. Внедрение PHI в номограмму ERSPCRC (European Randomized Study of Screening for Prostate Cancer Risk Calculator) также улучшило прогнозирование клинически значимого РПЖ (AUC 0,78 против 0,72, p=0,04) [23].
В настоящее время анализ PHI предоставляет прогностическую информацию как самостоятельный метод диагностики и скрининга. PHI может быть полезным как для включения пациентов в группу активного наблюдения, так и для отслеживания динамики заболевания и определения показаний к проведению повторной биопсии [3].
4Кscore
4Kscore определяется по уровню четырех калликреинов в сыворотке крови: оПСА, свПСА, интактного ПСА и калликреина-2 в сочетании с клинической информацией (возраст, данные ПРИ, результат биопсии). 4Kscore позволяет прогнозировать риск наличия у пациента агрессивного РПЖ (сумма баллов по шкале Глисона ≥7) [17].
D. Lin и соавт. [24] было проведено проспективное мультицентровое исследование (Canary PASS), основной целью которого стало сравнение эффективности 4Kscore и ПСА в прогнозировании РПЖ высокой степени злокачественности у больных, находящихся под активным наблюдением. Оценка конечного результата учитывала повышение суммарного балла по шкале Глисона (≥7) после первичной биопсии. По результатам обследования 718 пациентов показано, что использование 4Kscore позволяет с большей точностью прогнозировать повышение исходного балла Глисона (AUC 0,78 против 0,74) при второй биопсии. Сравнительная эффективность в прогнозировании повышения балла Глисона при последующих биопсиях не выявила преимуществ прогностической ценности 4Kscore по сравнению с ПСА (AUC 0,75 против 0,76).
Информативность 4Kscore в прогнозировании агрессивного РПЖ была оценена S. Zappala и соавт. [25]. Проспективное исследование было проведено в 26 урологических отделениях США с включением данных 1012 пациентов. 4Kscore был рассчитан для каждого пациента с/без учета данных ПРИ. Влияние данных ПРИ на прогностическую ценность метода оценено при помощи площади под кривой (AUC-ROC); оценка конечного результата включала выявление РПЖ с суммой баллов по Глисону ≥7. Агрессивный РПЖ был выявлен у 231 (23%) пациента, статистически значимой разницы между моделями 4Kscore с ПРИ и без ПРИ не было обнаружено (AUC 0,821 против 0,818).
Сравнительный анализ показал, что решение по поводу биопсии предстательной железы, принятое на основании данных 4Kscore, было ассоциировано с большей экономической выгодой за счет уменьшения количества «ненужных» биопсий по сравнению с группой больных, перенесших биопсию на основании одного лишь ПСА [26].
Эффективность 4Kscore была оценена по сравнению с некоторыми калькуляторами риска РПЖ, такими как PCPTRC 2.0 (Prostate Cancer Prevention Trial Risk Calculator) и ERSPC-RC 4 (European Research Screening Prostate Cancer Risk Calculator 4) [27]. В исследование был включен 51 пациент, перенесший биопсию предстательной железы (минимум 10 точек) с последующей оценкой биоптатов четырьмя независимыми морфологами. У 22 (43%) пациентов при патоморфологическом исследовании был выявлен РПЖ, из них у 5 (23%) – высокой степени злокачественности. Вероятность обнаружения РПЖ значительно различалась между 4Kscore, PCPTRC 2.0 и ERSPC-RC 4 (p≤0,022).
В проспективное рандомизированное исследование ProtecT (Prostate Testing for Cancer and Treatment) [28] были включены 6129 пациентов с уровнем оПСА ≥3 нг/мл, перенесших биопсию простаты. В ходе проведенного исследования авторы пришли к выводу, что использование 4Kscore позволяет прогнозировать РПЖ высокой степени злокачественности (AUC 4Kscore 0,820, %свПСА 0,799 и оПСА 0,738, p<0,001). Используя пороговое значение 4Kscore, равное 6%, возможно избежать до 43% «ненужных» биопсий при пропуске только 11% случаев РПЖ высокой степени злокачественности.
TMPRSS2-ERG (T2:ERvG)
TMPRSS2 представляет собой андрогензависимый ген, специфичный для РПЖ. В большом количестве ген определяется в моче после ПРИ, а также в образцах ткани предстательной железы после биопсии и РПЭ. В мультицентровом исследовании, включившем данные 1312 мужчин, T2:ERG продемонстрировал бóльшую диагностическую точность, чем оПСА. Сам по себе этот метод мало информативен, но в сочетании с ПСА (≥10 нг/мл) и PCA3 Т2:ERG в несколько раз увеличивает вероятность диагностирования РПЖ [29, 30].
Доступный для клинического применения тест MiPS (Mi-Prostate Score) был разработан для прогнозирования риска развития РПЖ. Данный тест включает данные оПСА сыворотки крови, PCA3 и ТMPRSS2-ERG.
В 2016 г. S. Tomlins и соавт. [31] провели сравнительную оценку эффективности отдельных компонентов, входящих в состав теста MiPS, и PCPTRC в прогнозировании риска развития РПЖ. В исследование были включены 1244 пациента, у которых анализ мочи был собран после ПРИ. Показано, что тест MiPS в значительной степени превосходит оПСА и PCA3 (AUC 0,747, р<0,001), оПСА и T2:ERG (AUC 0,729, р<0,01), а также оПСА (AUC 0,651, р<0,001) в качестве единственного маркера РПЖ. Полученные данные были равноценными для пациентов с первичной и повторной биопсией. Комбинация MiPS–PCPTRC позволит избежать до 47% «ненужных» биопсий при пропущенных 1,0–2,3% случаев РПЖ.
MiPS является многообещающим и перспективным тестом для скрининга РПЖ, тем не менее для окончательного внедрения данного теста в клиническую практику необходимо проведение сравнительных исследований с другими биомаркерами, такими как PHI и 4Kscore.
SelectMDx
SelectMDx – это еще один коммерчески доступный тест, основанный на анализе двух генов мочи (HOXC6 и DLX1), используемый для выявления РПЖ высокой степени злокачественности (сумма Глисона ≥7). Существующие рекомендации подразумевают его применение пациентами, которым показана биопсия простаты или которые ранее имели отрицательные биопсии, несмотря на факторы риска РПЖ (изменения по данным ПРИ, наследственный фактор или высокий уровень оПСА). Данный тест был разработан L. Van Neste и соавт. [32] и в последующем оценен в когорте из 386 пациентов. Авторами показано, что до 42% биопсий можно было бы избежать, при этом было бы пропущено 2% случаев РПЖ с суммой баллов по шкале Глисона ≥7.
ConfirmMDx
ConfirmMDx является тканевым биомаркером, в основе которого лежит оценка трех биомаркеров, ассоциированных с РПЖ, – GSTP1, APC и RASSF1. Данный маркер позволяет выявлять клинически значимый РПЖ у пациентов с отрицательной биопсией. Имеющиеся данные свидетельствуют о том, что по уровню ConfirmMDx возможно прогнозировать риск обнаружения РПЖ при повторной биопсии с вероятностью до 90% [17].
В отличие от других коммерчески доступных маркеров, содержание которых оценивают в опухолевой ткани для принятия решения о необходимости лечения, ConfirmMDx является единственным маркером, с помощью которого можно прогнозировать вероятность РПЖ, при этом исследуя доброкачественную ткань. В рекомендациях NCCN (National Comprehensive Cancer Network) ConfirmMDx обозначен как дополнительный метод, позволяющий принять решение о целесообразности повторной биопсии. Вместе с тем на сегодняшний день отсутствуют исследования, сравнивающие ConfirmMDx с мпМРТ с позиций экономической выгоды [17, 33].
Эффективность ConfirmMDx в прогнозировании РПЖ была подтверждена в исследовании MATLOC (Великобритания–Бельгия), включившем 483 пациента с отрицательными результатами биопсии в анамнезе [34]. Отрицательная прогностическая ценность составила 90%. В работе [33] отрицательная прогностическая ценность ConfirmMDx составила 88%; авторы также сообщили о 2,5-кратном увеличении риска выявления РПЖ у пациентов (n=320) при повторной биопсии.
ELAVL1 и другие маркеры
ELAVL1 представляет собой РНК-связывающий белок, продуцируемый в различных тканях, в том числе в предстательной железе; является независимым прогностическим биомаркером у больных РПЖ, показателем неблагоприятного фенотипа опухоли либо раннего рецидива РПЖ после проведенного лечения [35]. Проведенные экспериментальные исследования in vitro на культуре клеток предстательной железы позволили открыть новые биомаркеры РПЖ. Доказана роль ряда белков человеческого организма, таких как CD151, DIAPH3, Runx2 и многие другие, в ранней диагностике РПЖ, определении показаний к проведению повторной биопсии и риска развития агрессивного РПЖ [36].
Заключение. Несмотря на высокие темпы развития методов лабораторной диагностики РПЖ, по-прежнему одной из самых актуальных проблем при выявлении рака остается сложность частой визуализации опухолевых очагов. Как следствие – биопсия предстательной железы выполняется лишь на основании повышенного уровня ПСА и данных ПРИ, что далеко не всегда позволяет дифференцировать суспициозные участки и забор материала производится из стандартных зон. Существующая альтернатива – биопсия под контролем МРТ, однако присущие временные и финансовые затраты налагают существенные ограничения на широкое использование данной методики.
Внедрение новых биомаркеров позволяет создавать персонализированный подход к диагностике, лечению и прогнозированию течения РПЖ у каждого конкретного пациента. В связи с отсутствием стандартизированных алгоритмов использования, необходимой аппаратуры и специалистов некоторые из перечисленных в данной статье методы ранней диагностики РПЖ остаются недоступными. Остальные, несмотря на высокую прогностическую ценность, зачастую имеют малую чувствительность и специфичность. Проведение мультицентровых клинических исследований, направленных на оценку актуальности и перспектив повсеместного внедрения в клиническую практику, позволит определить место новых методов диагностики РПЖ в ряду «золотого» стандарта наряду с определением уровня ПСА и биопсией предстательной железы под контролем ТРУЗИ.
Работа выполнена при поддержке РНФ, соглашение № 16-19-10567


