Введение. Во многих эпидемиологических исследованиях показана прямая связь между сексуальной активностью и продолжительностью жизни мужчин [1]. Значительное число мужчин среднего и пожилого возраста имеют различные сердечно-сосудистые заболевания (ССЗ) [2–4]. В последние годы появляется все больше публикаций, посвященных взаимосвязи факторов риска ССЗ с половыми расстройствами [2, 5–9].
Ингибиторы фосфодиэстеразы 5-го (ФДЭ-5) являются наиболее эффективными средствами медикаментозной терапии эректильной дисфункции (ЭД) [10]. Высокая эффективность силденафила отмечена в разных возрастных группах [11–15].
Среди пациентов, которые подвергаются трансуретральной резекции (ТУР) доброкачественной гиперплазии предстательной железы (ДГПЖ), большинство составляют мужчины пожилого возраста. Однако многие из них в понятие «улучшение качества жизни» вкладывают улучшение качества не только мочеиспускания, но и сексуальной жизни.
В связи с чем нами проведено исследование, целью которого стало изучение эффективности и безопасности применения силденафила больными с ЭД и сопутствующими ССЗ, перенесшими ТУР предстательной железы по поводу ее доброкачественной гиперплазии.
Материалы и методы. В исследование были включены 59 пациентов (возраст от 50 до 75 лет) с диагнозом «доброкачественная гиперплазия предстательной железы», нуждающихся в оперативном лечении, живущих половой жизнью, но имеющих ЭД и сопутствующие ССЗ. Для всех пациентов, включенных в исследование, допускался прием препаратов группы ингибиторов ангиотензинпревращающего фермента, β-адреноблокаторов, антагонистов кальция.
Критерии включения:
- объем предстательной железы 60–80 см3;
- неэффективность консервативного лечения;
- балл по шкале IPSS более 20;
- показатель Международного индекса эректильной функции (МИЭФ) менее 21;
- наличие одного или более заболеваний сердечно-сосудистой системы (контролируемая артериальная гипертензия (АГ) 1–2-й степени, ИБС – стабильное течение (стенокардия напряжения I–II функциональных классов [ФК]);
- письменное информированное согласие пациента.
Критерии невключения:
- высокий сердечно-сосудистый риск;
- АГ 3-й степени, неконтролируемая АГ;
- хроническая сердечная недостаточность III–IV ФК;
- нестабильная стенокардия;
- перенесенные за последние 6 мес. инфаркт миокарда и острое нарушение мозгового кровообращения;
- необходимость приема нитратов;
- декомпенсация функций печени и/или почек и/или других жизненно важных органов;
- урологические заболевания в острой стадии;
- отсутствие половой жизни;
- объем предстательной железы более 80 см3;
- неспособность адекватно отвечать на вопросы исследователя, заполнять необходимые документы и применять исследуемые препараты;
- участие в исследовании какого-либо другого лекарственного препарата и/или метода лечения;
- индивидуальная непереносимость силденафила;
- андрогенный дефицит.
Пациентам, соответствовавшим критериям включения, разъясняли характер предстоящего исследования и связанных с ним мероприятий. До включения в исследование пациенты подписывали информированное согласие, приложенное к индивидуальной карте больного.
Все пациенты, включенные в исследование, в соответствии с планом рандомизации были разделены на две группы, сопоставимые по возрасту, клиническим проявлениям, степени выраженности, предположительной этиологии и патогенезу ЭД: группу сравнения (n=29) и основную группу (n=30). В качестве контрольной группы мы использовали данные обследований здоровых мужчин возрастом от 25 до 35 лет (средний возраст – 28±3,3 года).
Всем пациентам обеих групп была проведена биполярная ТУР ДГПЖ. После операции пациентам назначены тамсулозин 0,4 мг 1 раз в сут. на 90 дней, ципрофлоксацин по 500 мг 2 раза в сут. на 10 дней. Помимо этого пациенты принимали препараты в обычном режиме по поводу сопутствовавшей терапевтической патологии. Пациенты основной группы с 30-го дня после операции получали силденафил (ЭФФЕКС Силденафил Эвалар) по 50 мг ситуационно за 1–2 ч до полового акта в течение 60 дней. Данный препарат был выбран нами с позиций экономической обоснованности.
Протокол исследования предусматривал три визита.
На визите 1 пациент подписывал информированное согласие на участие в исследовании; проводились сбор жалоб, анамнеза и физикальный осмотр пациента, регистрация данных инструментальных и лабораторных методов исследований, оценивалась необходимость проведения оперативного вмешательства.
В ходе визита 2, который проходил через 30 дней после операции, исследователь проводил регистрацию нежелательных явлений, симптомов ДГПЖ и эректильной дисфункции, анкетирование по шкалам МИЭФ и IPSS.
На визите 3 (на 90-й день после ТУР ДГПЖ) регистрировали нежелательные явления, симптоматику ДГПЖ и эректильной дисфункции, выполняли анкетирование по шкалам МИЭФ и IPSS, осуществляли забор крови и мочи с целью проведения анализов. Проводили исследование гемодинамики предстательной железы при помощи ультразвуковой допплерографии в импульсно-волновом режиме. При динамическом исследовании в режиме цветного сканирования выбирался сосуд с оптимальными визуальными параметрами, которые позволяли определять этот сосуд как один из магистральных и производить запись допплеровского спектра с качеством, пригодным для анализа. Такими параметрами служили крупный диаметр сосуда (в среднем 0,072±0,004 см в диаметре), наличие в проксимальном его отделе более мелких ветвей, отсутствие извитости сосуда и расположение его под острым углом (менее 70⁰) к оси сканирования.
Микроциркуляцию оценивали с помощью лазерной допплеровской флоуметрии в точке проекции предстательной железы с помощью накожного зонда, работающего через инфракрасный канал. Зонд устанавливался в биологически активной точке, которая располагается по передней срединной линии промежности между мошонкой и анусом. Измерения проводились на аппарате ЛАКК-02 (НПП «Лазма», Москва) с помощью программного обеспечения LDF 1,18.
В течение всего периода наблюдения пациенты вели дневник гемодинамики, в котором регистрировали показатели АД и ЧСС 2 раза в сутки планово, а также до и через 15 мин после полового акта.
Пациент мог быть исключен из исследования по следующим причинам:
- возникновение серьезных нежелательных эффектов, приведших к временной потере трудоспособности;
- нарушение протокола пациентом или исследователем;
- по усмотрению исследователя, если тот считал, что продолжение исследования наносит вред здоровью пациента;
- по желанию самого пациента.
 В работе использованы различные методы статистической обработки в зависимости от типа случайных величин и поставленной задачи исследования: t-критерий Стьюдента, критерий Манна–Уитни (для независимых выборок) и T-критерий Вилкоксона (для связанных выборок) [16]. Во всех случаях использовали двусторонние варианты критериев. Обработку и графическое представление данных проводили с помощью компьютерных программ Statistica 6.0 и Excel 2003.
В работе использованы различные методы статистической обработки в зависимости от типа случайных величин и поставленной задачи исследования: t-критерий Стьюдента, критерий Манна–Уитни (для независимых выборок) и T-критерий Вилкоксона (для связанных выборок) [16]. Во всех случаях использовали двусторонние варианты критериев. Обработку и графическое представление данных проводили с помощью компьютерных программ Statistica 6.0 и Excel 2003.
Результаты. Средний возраст пациентов составил 63,4±5,3 года, объем предстательной железы – 69,7±5,9 см³ (от 65,8 до 78,4 см³). Явлений гипогонадизма выявлено не было, уровень общего тестостерона составил 18,67±5,34 нмоль/л. Артериальная гипертензия диагностирована у всех 59 (100%) пациентов, ИБС – у 29 (49%). Макрогемодинамику в предстательной железе оценивали методом трансректального УЗИ с цветовым допплеровским картированием.
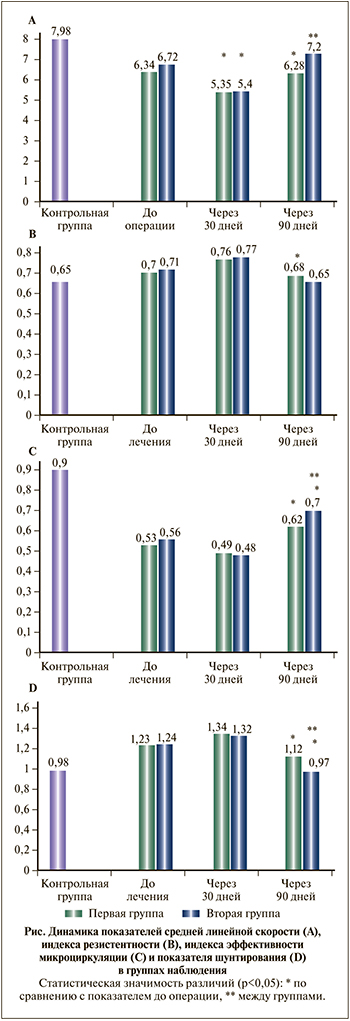
До лечения у пациентов обеих групп отмечено снижение линейной средней скорости кровотока, индекса эффективности микроциркуляции с одновременным повышением индекса резистентности и показателя шунтирования по сравнению с группой здоровых мужчин (см. рисунок). Данные нарушения мы связываем с наличием аденоматозной ткани, сдавлением артерий и венозным застоем. По прошествии 30 дней после операции у пациентов обеих групп констатировали усугубление гемодинамических нарушений (см. рисунок), что может быть связано с послеоперационными изменениями в ложе простаты. У пациентов основной группы через 90 дней после операции отмечено наиболее выраженное улучшение макрогемодинамики и микроциркуляции в предстательной железе, что проявлялось достоверным повышением средней линейной скорости и снижением индекса резистентности. Данные показатели приблизились к значениям группы здоровых мужчин. Эти изменения мы объясняем возможностью ингибиторов ФДЭ-5 улучшать артериальный кровоток не только в пенильных артериях, но и в артериях органов таза, в том числе предстательной железы, а также положительно влиять на микроциркуляцию в органах малого таза.
У пациентов группы сравнения через 90 дней после операции изменения гемодинамики и микроциркуляции в предстательной железе на фоне лечения были недостоверными (см. рисунок).
При оценке эректильной функции с помощью индекса МИЭФ до операции у пациентов группы сравнения средний балл составил 12±0,52, что свидетельствует об умеренной ЭД. Через 60 дней после операции средний балл достоверно не изменился и составил 11±0,46. У пациентов основной группы до операции также были выявлены умеренные нарушения эректильной функции – 11±0,63 балла, однако через 60 дней после операции (прием силденафила по 50 мг ситуационно в течение 60 дней) отмечено статистически значимое увеличение индекса МИЭФ до 22,34±0,72 (отсутствие ЭД), что расценено нами как очень хороший клинический эффект.
Средняя оценка по шкале IPSS пациентов группы сравнения до операции составила 24,82±0,67 балла, через 30 дней после ТУР ДГПЖ – 15,38±0,72, через 90 дней после операции – 10±0,45 балла. У пациентов основной группы показатели на указанных сроках наблюдения составили 25,46±0,64, 16,25±0,45 и 7,2±0,36 балла соответственно. Данный факт мы расцениваем как влияние силденафила на кровоток детрузора и возможную способность уменьшать гипоксию и ишемические явления.
Согласно данным дневников гемодинамики, применение силденафила не сопровождалось статистически значимыми изменениями как систолического, так и диастолического АД, а также ЧСС после полноценного полового акта по сравнению с группой пациентов, не получавших ингибитора ФДЭ-5. Полученные результаты свидетельствуют о том, что среди мужчин с ЭД с сопутствующими ССЗ, получавших антигипертензивную терапию (независимо от дозировки или класса препарата), профиль нежелательных явлений в целом был такой же, как и у мужчин без сердечно-сосудистых заболеваний, получавших силденафил.
Переносимость препарата. За время исследования никаких аллергических реакций ни в одной группе не отмечено.
Нежелательные явления. Негативных изменений в общем состоянии пациентов, появления новых жалоб, патологических отклонений лабораторных показателей (общего и биохимического анализов крови и общего анализа мочи) в ходе исследования не зафиксировано.
Выводы
1. Важно и необходимо оценивать половую функцию у мужчин с ССЗ, перенесших ТУР ДГПЖ.
- Силденафил (ЭФФЕКС Силденафил Эвалар) улучшает эректильную функцию у пациентов с ССЗ, подвергшихся ТУР ДГПЖ.
- Силденафил в дозировке 50 мг при ситуационном приеме не оказывает отрицательного влияния на основные показатели гемодинамики (АД, ЧСС) у пациентов с ССЗ после оперативного лечения по поводу ДГПЖ.
- В долгосрочной перспективе в ведении пациентов данной категории следует придерживаться стратегии, направленной на выявление и коррекцию основных факторов риска развития и прогрессирования ССЗ.



