Введение. Пролапс тазовых органов с разной степенью выраженности наблюдается у 50% женщин после родоразрешения естественным путем, а у 10–20% пациенток он имеет выраженную стадию, требующую оперативного лечения [1–3].
Это состояние негативно влияет на качество жизни женщин, в том числе в интимной сфере, и социальную адаптацию [4–8].
Ухудшение качества жизни усугубляют симптомы со стороны нижних мочевых путей. В зависимости от стадии и индивидуальных особенностей пролапса у женщины это могут быть как недержание мочи при напряжении, так и обструктивное мочеиспускание, вплоть до полной задержки мочеиспускания.
Изменение нормального положения мочевого пузыря часто сопровождается появлением остаточной мочи в мочевом пузыре, нарушением пассажа мочи по мочеточникам и как следствие – развитием гидронефроза. Наличие остаточной мочи приводит к инфицированию мочевых путей, а выраженная и длительно существующая обструкция верхних мочевых путей может сопровождаться тяжелым рецидивирующим воспалительным процессом в почках [9–14].
Применение синтетических сетчатых имплантатов при трансвагинальной реконструкции тазового дна позволяет достигать хороших анатомических результатов [15].
Часть пациенток имеют так называемое оккультное, или скрытое, недержание мочи при выраженном пролапсе, и у них после реконструктивных операций появляется клиника стрессового недержания мочи de novo. Объясняется это устранением «перегиба» мочевого пузыря в области шейки его, что являлось механизмом удержания мочи в условиях пролапса тазовых органов. Это состояние в большинстве случаев требует дополнительной операции для устранения стрессового недержания мочи.
В рекомендациях AUA (American Urological Association – американской урологической ассоциации) 2011 г. говорится о безопасности выполнения одновременных операций для коррекции пролапса и стрессового недержания мочи у правильно отобранных женщин (при правильном определении показаний), однако также указывается на отсутствие единого мнения о профилактической анти-стрессовой операции при выраженном пролапсе [16].
В настоящее время нет стандартизированной техники точной диагностики скрытой инконтиненции, как и нет единого мнения о показаниях и необходимости выполнения реконструктивной и антистре ссовой операции одномоментно [17].
Таким образом, целесообразно ли при сочетании пролапса гениталий со стрессовой формой недержания мочи наряду с реконструкцией тазового дна выполнять уретропексию, а тем более превентивно, остается открытым вопросом, актуальным для дальнейшего изучения.
Цель исследования. Определить целесообразность одномоментного выполнения трансвагинальной реконструкции тазового дна сетчатыми имплантатами и петлевой уретропексии при стрессовом недержании мочи, как сопутствующем пролапсу тазовых органов, так и возникшем после реконструктивной операции по поводу тазового пролапса.
Материалы и методы. Проанализированы результаты обследования и оперативного лечения 206 пациенток с пролапсом тазовых органов III и IV стадий.
В зависимости от наличия или отсутствия стрессового недержания мочи пациентки разделены на 2 группы.
Первую группу составили 72 женщины, у которых пролапс тазовых органов III и IV стадий сопровождался стрессовым недержанием мочи. Во всех случаях выполнена операция – трансвагинальная реконструкция тазового дна с использованием сверхлегких сетчатых эндопротезов из полипропилена. Девяти пациенткам эта операция выполнена одномоментно с трансобтураторной уретропексией сетчатой полипропилен-поливинилиденфторидной эндопротезом-лентой.
Вторую группу составили 134 женщины, у которых пролапс тазовых органов III и IV стадий не сопровождался клиникой стрессового недержания мочи. Этим пациенткам выполнена такая же реконструктивная операция, в 10 наблюдениях одномоментно с трансобтураторной уретропексией. К применению такого подхода нас побудило возникновение стрессовой формы недержания мочи de novo после трансвагинальной реконструкции таза, а также рекомендации AUA.
Все пациентки обследованы трижды до операции и через 1 и 12 месяцев после нее.
Обследование включало изучение жалоб, анамнеза заболевания и жизни, оценку субъективных симптомов и качества жизни по анкете-опроснику SEAPI [18, 19], общего и урогинекологического осмотра, лабораторных исследований, проведения ультразвукового исследования органов малого таза и почек, урофлоуметрии. Урогинекологический осмотр женщины на гинекологическом кресле являлся основным исследованием для постановки диагноза, определения стадии пролапса, объема оперативного лечения и диагностики стрессового недержания мочи.
Стадию пролапса определяли согласно классификации Baden-Walker, 1972 [20]. В случае выявления расширения верхних мочевых путей по результатам УЗИ пациенткам выполняли экскреторную урографию с нисходящей цистографией с целью определения причины, уровня и характера обструкции. После операции оценивали анатомический эффект, качество жизни пациенток, устранение обструктивных симптомов верхних и нижних мочевых путей, а также стрессового недержания мочи.
Результаты. Результаты обследования пациенток обеих групп до операции. При изучении клинических симптомов пациенток нами установлено, что обструктивная симптоматика встречалась среди большинства пациенток – 119 (57,8%) из 206. Семьдесят две (35%) пациентки имели клинику недержания мочи при напряжении, они составили первую группу, 15 (7,2%) при имеющемся пролапсе тазовых органов III и IV стадий не отмечали затруднений при мочеиспускании и недержания мочи.
При анализе анкет-опросников SEAPI среднее значение суммы симптомов составило 26,5±14,9, индекса качества жизни – 5,5±0,5 баллов.
Лейкоцитурия при первичном обследовании отмечена у 107 (51,9%) из 206 женщин, в основном у пациенток с обструктивной симптоматикой и наличием остаточной мочи.
У 16 (7,8%) пациенток выявлено расширение чашечно-лоханочной системы почек, им выполнена экскреторная урография с нисходящей цистографией, по результатам которой установлено, что причиной гидронефроза стало изменение анатомии тазового дна (опущение мочевого пузыря и как следствие – нарушение пассажа мочи по мочеточникам на уровне предпузырных отделов). В выявленных наблюдениях с обструктивной симптоматикой встречался как односторонний, так и двусторонний уретерогидронефроз I–III степеней.
При анализе результатов урофлоуметрии установлено, что у пациенток, предъявивших жалобы на затруднения при мочеиспускании, получены кривые, соответствующие обструктивному типу мочеиспускания и отмечено уменьшение максимальной, средней скорости мочеиспускания, а также объема мочи при мочеиспускании. У пациенток, имевших клинику недержания мочи при напряжении, и у пациенток с бессимптомным пролапсом при урофлоуметрии были получены кривые, характерные для нормального мочеиспускания, однако значения максимальной и средней скорости мочеиспускания также были снижены. Среднее значение максимальной скорости мочеиспускания составило 10,21±4,54 мл/с, средней скорости мочеиспускания – 4,7±2,0 мл/с, времени мочеиспускания – 40,6±10,0 с, объема мочи при мочеиспускании – 114,6±31,2 мл.

Также у пациенток с обструктивной симптоматикой при ультразвуковом исследовании мочевого пузыря определялась остаточная моча, объем которой варьировался от 40 до 310 мл, среднее значение – 130,4±90,0 мл.
При урогинекологическом осмотре установлено, что у 79 (38,3%) пациенток имеется пролапс тазовых органов III, у 127 (61,7%) – IV стадий.
Также отмечено, что при III стадии пролапса чаще встречается клиника стрессовой формы недержания мочи – 41 из 79 (51,9%) больных, чем при IV стадии – 31 из 134 (23,1%). В связи с этим в первую группу (POP+SUI, n=72) вошли 52 (65,8%) женщины с пролапсом III стадии и 20 (34,2%) – IV стадии, а во вторую (POP, n=134) 27 (20,1%) и 107 (79,9%) соответственно. У 10 пациенток второй группы, не отмечавших недержания мочи, после устранения пролапса мы зафиксировали резко положительную кашлевую пробу (оккультное недержание мочи), у них мы обосновали одномоментное выполнение реконструкции тазового дна и уретропексии.
Оценка результатов оперативного лечения пациенток обеих групп. Через 1 мес после операции анализ повторно заполненных анкет-опросников SEAPI выявлено статистически достоверное уменьшение суммы симптомов (с 26,5±14,9 до 8,9±4,3) и индекса качества жизни (с 5,5±0,5 до 1,2± 0,4). Число наблюдений лейкоцитурии также значительно снизилось: с 107 (51,9%) наблюдений исходно до 21 (10,2%) при контроле.
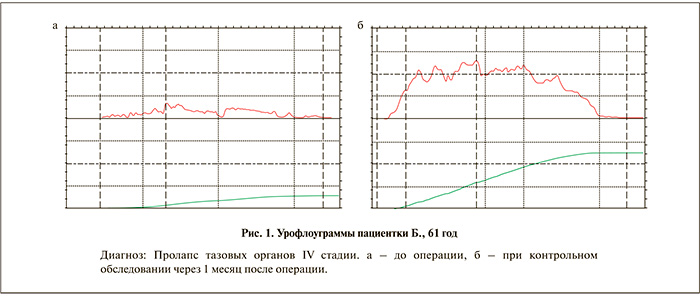
Все пациентки с обструктивным мочеиспусканием отмечали регресс симптомов после операции. Отсутствие обструктивной симптоматики подтверждалось данными урофлоуметрии и уменьшением объема остаточной мочи, оцененным при помощи ультразвукового исследования. Среднее значение максимальной скорости мочеиспускания составило 16,45±4,72 мл/с, средней скорости мочеиспускания – 7,4±3,1 мл/с, времени мочеиспускания – 21,1±7,3 с, объема мочи при мочеиспускании – 210,2±30,6 мл. Также при ультразвуковом исследовании мочевого пузыря отмечено отсутствие клинически значимого количества остаточной мочи, среднее значение – 15,0±10,0 мл. На рис. 1 приведены урофлоуграммы пациентки, полученные до операции и при контрольном обследовании.
При контрольном ультразвуковом исследовании почек отмечено, что у пациенток с ранее выявленным уретерогидронефрозом зафиксирован регресс дилатации чашечно-лоханочных систем почек.
Анатомическая эффективность достигнута у 203 (98,5%) из 206 женщин. На рис. 2 приведены фотографии, сделанные при урогинекологическом осмотре одной из пациенток до и после операции, иллюстрирующие анатомическую эффективность трансвагинальной реконструкции тазового дна. При урогинекологическом осмотре через год у 3 (1,5%) пациенток из 206 диагностирован рецидив тазового пролапса. До операции все эти пациентки имели пролапс IV стадии, после операции в одном наблюдении отмечен рецидив до III стадии, в двух до исходного состояния – IV стадии.
Все выше представленные данные статистически не различались в группах, поэтому приводятся для обеих групп вместе.
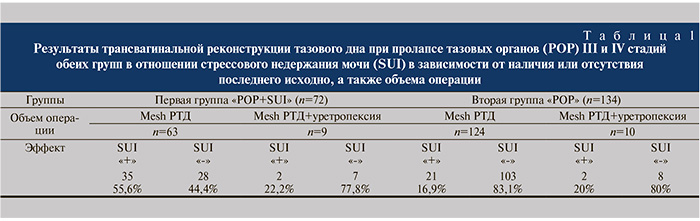
Результаты, полученные через месяц после оперативного лечения в отношении стрессовой инконтиненции в обеих группах пациенток представлены в табл. 1.
Как видно из таблицы у пациенток с исходно сопутствующим стрессовым недержанием мочи при выполнении только реконструктивной операции в 44,4% (28 из 63) удалось ликвидировать инконтиненцию, а в 55,6% (35 из 63) она сохранилась. При одномоментной реконструктивной и петлевой операции у пациенток с исходно сопутствующим стрессовым недержанием мочи ликвидировать инконтиненцию удается в 77,8% (7 из 9) наблюдений.
В группе пациенток с пролапсом гениталий без недержания мочи после реконструктивной операции по поводу тазового пролапса стрессовая инконтиненция de novo возникла у 21 (16,9%) пациентки из 124. У женщин с диагностированным до операции оккультным недержанием мочи при выполнении одномоментной реконструктивной и петлевой операции в 20% (2 из 10) отмечается недержание мочи после операции, у 8 из 10 эффективна.
В ходе дальнейшего наблюдения за пациентками с сохраняющейся стрессовой формой инконтиненции и возникшей вновь отмечено, что недержание мочи, диагностированное через месяц после операции, с течением времени не купируется. Всем этим пациенткам в сроки от 3 до 12 мес после первой операции выполнена петлевая уретропексия с положительным результатом.
Обсуждение. По полученным нами данным, трансвагинальная реконструкция тазового дна с использованием синтетических сетчатых имплантов позволила обеспечить хорошие анатомические результаты (203 из 206 – 98,5%), что соответствует данным литературы [15].
Анализ результатов оперативного лечения значительного числа больных пролапсом тазовых органов с разной клинической картиной и применением разных тактик показал, что нецелесообразно одномоментно выполнять трансвагинальную реконструкцию тазового дна сетчатым имплантом и петлевую уретропексию ни пациенткам с сопутствующим пролапсу гениталий стрессовым недержанием мочи, ни пациенткам с выраженной степенью пролапса для профилактики оккультного недержания мочи. Двадцати восьми (44,4%) из 63 женщин реконструкция тазового дна без одномоментной уретропексии позволила устранить сопутствующее пролапсу гениталий стрессовое недержание мочи.
С другой стороны, несмотря на привлекательность одномоментного устранения пролапса и инконтиненции или профилактики последней, сочетание этих методик не обеспечивает положительного результата в отношении инконтиненции во всех случаях. Последовательное же выполнение этих пособий обеспечивает лучшие отдаленные результаты. Предположительно мы объясняем это тем, что во время выполнения реконструктивной операции, вероятно, не удается обеспечить «правильное» расположение и натяжение сетки-петли под уретрой, ввиду того, что окончательные анатомические ориентиры тазового дна для проведения петли сформируются только по истечении 2–3 месяцев после реконструктивной операции по поводу тазового пролапса.
Заключение. Трансвагинальная реконструкция тазового дна с использованием синтетических сетчатых имплантов позволяет получать хорошие анатомические результаты: ряду больных устранить сопутствующее пролапсу гениталий стрессовое недержание мочи, а также всем пациенткам устранить обструктивные симптомы мочеиспускания, восстановить уродинамику нижних и верхних мочевых путей, а как следствие – снизить частоту и тяжесть осложнений инфекционно-воспалительного характера.
Оптимальной тактикой в отношении стрессовой формы недержания мочи в сочетании с пролапсом гениталий или появившимся после реконструктивной операции является петлевая уретропексия, выполненная после окончательной фиксации сетчатого импланта, установленного для коррекции тазового пролапса.
Считаем нецелесообразным одномоментно выполнять реконструктивные операции при пролапсе тазовых органов и петлевые уретропексии для устранения или профилактики стрессового недержания мочи.



