Введение. Доля бесплодных браков составляет 15–19% и в половине случаев обусловлена «мужским фактором» [1–4]. Одно из лидирующих мест в структуре причин негативного влияния на сперматогенез занимает хронический простатит [5, 6]. Поражая мужчин сравнительно молодого возраста (20–40 лет), простатит нередко становится причиной мужского бесплодия. За последние годы обращает на себя внимание рост заболеваемости хроническим простатитом как в России, так и в других странах. Это связано с широким распространением малоподвижного образа жизни, ухудшением экологической обстановки, бесконтрольным применением лекарственных препаратов, аллергизацией населения, вредными условиями труда [7, 8].
Многообразие клинических проявлений болезни, наличие осложнений, влияющих на репродуктивное здоровье мужчины, сложность диагностики, а также не всегда удовлетворительные результаты лечения придают вопросам диагностики и лечения простатита всевозрастающую социальную значимость [9].
 Все это заставляет ученых искать новые препараты для лечения простатита и совершенствовать уже имеющиеся методы этиотропной и патогенетической терапии. За последние годы при заболеваниях предстательной железы стали применять препараты биологического происхождения, выделенные из предстательной железы крупного рогатого скота. Было доказано, что эти препараты оказывают органотропное действие, т.е. влияют на процессы дифференцировки в популяции клеток, из которых они выделены. Кроме того, они обладают противовоспалительным и иммуномодулирующим эффектами, влияют на показатели гемостаза, усиливают синтез антигистаминовых и антисеротониновых антител и улучшают микроциркуляцию в пораженном органе [10].
Все это заставляет ученых искать новые препараты для лечения простатита и совершенствовать уже имеющиеся методы этиотропной и патогенетической терапии. За последние годы при заболеваниях предстательной железы стали применять препараты биологического происхождения, выделенные из предстательной железы крупного рогатого скота. Было доказано, что эти препараты оказывают органотропное действие, т.е. влияют на процессы дифференцировки в популяции клеток, из которых они выделены. Кроме того, они обладают противовоспалительным и иммуномодулирующим эффектами, влияют на показатели гемостаза, усиливают синтез антигистаминовых и антисеротониновых антител и улучшают микроциркуляцию в пораженном органе [10].
Витапрост служит ярким представителем данной группы препаратов, зарекомендовавшим себя как высокоэффективное и безопасное средство лечения заболеваний предстательной железы. Активным веществом витапроста является эндогенная субстанция сампрост (простаты экстракт) – комплекс водорастворимых биологически активных пептидов, выделенных из предстательной железы ткани простаты крупного рогатого скота [11, 12].
При планировании настоящего исследования были поставлены основная, первичная и вторичная цели.
Основной целью данного исследования стало изучение влияния терапии витапростом в форме ректальных суппозиториев и витапростом в форме таблеток на сперматогенез у пациентов с бесплодием, развившимся на фоне хронического простатита.
Первичной целью исследования было оценить степень уменьшения выраженности болевого синдрома при лечении витапростом в различных формах выпуска, вторичной целью – оценка переносимости и безопасности препаратов на основе анализа нежелательных явлений.
Материалы и методы. В исследование были включены 30 мужчин в возрасте 18–50 лет, находящихся на амбулаторном лечении с диагностированным бесплодием, развившимся на фоне хронического простатита, с имеющимися патологическими изменениями в спермограмме (секреторно-токсическая форма бесплодия). К обязательным условиям включения в исследование относятся отсутствие патологической флоры при микроскопическом исследовании эякулята, секрета предстательной железы и отрицательный результат ПЦР на хламидии, микоплазмы, уреаплазмы и гарднереллы. Уровень простатспецифического антигена (ПСА) в плазме крови был в пределах референсных значений. В исследование вошли только те пациенты, в отношении которых были исключены все другие патологические процессы, кроме хронического простатита, влияющие на сперматогенез. Ни один из пациентов, включенных в исследование, ранее не получал терапию витапростом.
Все больные получали терапию препаратом витапрост (суппозитории ректальные 50 мг) по 1 суппозиторию 1 раз в сутки. Длительность курса лечения составила 30 дней. Затем лечение было продолжено препаратом витапрост в форме таблеток 100 мг внутрь (по 1 таблетке 2 раза в день). Длительность курса лечения препаратом витапрост в форме таблеток составила 40 дней. После приема препарата пациенты находились под наблюдением в течение 10 дней. Исследование проводилось в течение 80 дней в ходе 5 визитов, на 1-е, 15, 30, 70 и 80-е дни. Выполняли комплекс физикальных, инструментальных и клинико-лабораторных методов обследования. Изучали анамнез заболевания, проводили оценку симптомов хронического простатита с помощью общепринятой шкалы NIH-CPSI.
В качестве параметров эффективности терапии были выбраны положительная динамика в показателях анализа эякулята, снижение выраженности симптомов хронического простатита, уменьшение объема предстательной железы по данным трансректального УЗИ, оценка эффективности терапии врачом и пациентом. Влияние терапии на сперматогенез оценивали на основании данных стандартной спермограммы (ВОЗ, 2010).
Результаты исследований были обработаны общепринятыми методами статистики. Оценку значимости различий средних значений в независимых выборках определяли с использованием t-критерия Стьюдента (для количественных признаков при нормальном распределении данных и равенстве дисперсий), непараметрических критериев Манна–Уитни, двухвыборочного критерия Колмогорова–Смирнова (для количественных показателей при распределении, отличном от нормального или различных дисперсиях), относительных частот по критерию χ2 с поправкой Йетса (для качественных признаков). Разницу между средними значениями показателей считали значимой при р<0,05.
Центральные тенденции и рассеяния количественных признаков, имеющих приближенно нормальное распределение, описывали средним значением (М) и средним квадратичным отклонением (s) в формате M±s. Центральные тенденции и дисперсии количественных признаков, не имеющих приближенно нормального распределения, описывали медианой и интерквартильным размахов (25-й и 75-й перцентили) [13].
Результаты. Средний возраст участников исследования (медиана и интерквартильный размах) составил 35 лет (от 24 до 43 лет).
В ходе исследования клинически значимых отклонений показателей общих анализов крови и мочи не выявлено.
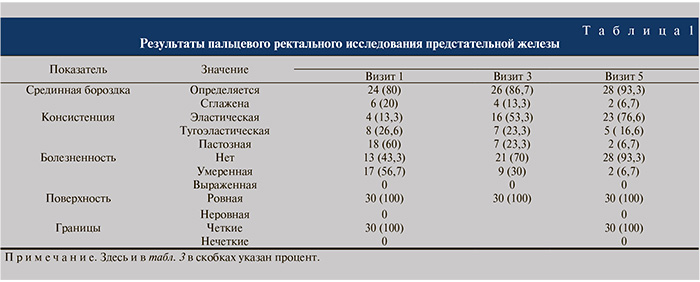
Одним из параметров оценки терапевтического эффекта проводимой терапии были данные пальцевого ректального исследования предстательной железы.
Как видно из табл. 1, число пациентов со сглаженностью срединной бороздки, свидетельствующей об отеке тканей простаты, к концу лечения уменьшилось на 13,3 %. Значимо уменьшалась болезненность предстательной железы – на 50 % к визиту 5.
Данные трансректального УЗИ простаты являлись одним из параметров эффективности, используемых для оценки терапевтического эффекта терапии и степени выраженности воспалительного процесса в предстательной железе.
На фоне приема витапроста к визиту 5 было достигнуто незначительное, но статистически достоверное снижение объема предстательной железы (в среднем на 9,40 см3): на визите 1 данный показатель составил 28,65±7,35 (15,3–36,5) см3, визите 3 – 21,47±6,21 (15,2–28,4) см3, визите 5 – 19,25±5,34 (14,3–24,5) см3. Данные изменения можно объяснить уменьшением или исчезновением отека ткани органа и нормализацией микроциркуляции в предстательной железе.
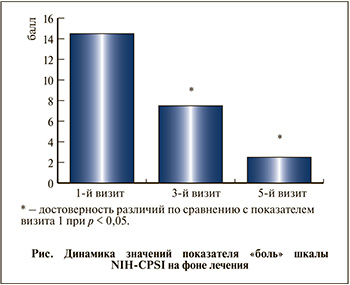
При оценке выраженности симптомов хронического простатита и тазовых болей по шкале NIH-CPSI выявлены статистически значимые (p<0,05) различия по показателю «боль» (рис. 1).
Немаловажную роль играет и оценка пациентом качества жизни. На фоне терапии выявлено достоверное снижение средних значений оценки качества жизни от визита 1 к визиту 3 и 5, составивших 6,5±2,3 (2–11), 3,6±1,2 (0–5) и 2,2±3,2 (0–3) (p<0,05 по сравнению с визитом 1) балла соответственно.
Основным параметром эффективности терапии послужило изменение показателей эякулята (табл. 2).
До лечения концентрация сперматозоидов в эякуляте была снижена и составила 22 млн в 1 мл.
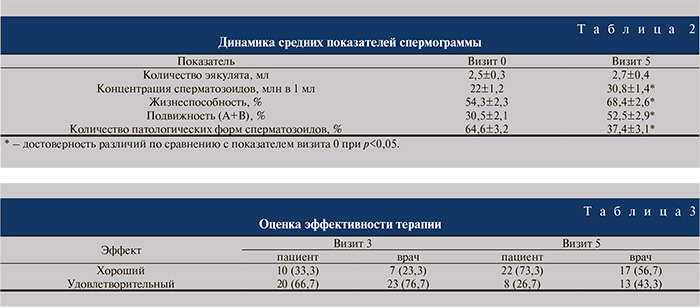
К визиту 5 значимо увеличились количество сперматозоидов, подвижность сперматозоидов (на 22%) и их жизнеспособность (14,1%). Количество патологических форм сперматозоидов к окончанию исследования уменьшилось на 27,2%. Данные изменения можно объяснить простатотропным и спермопротективным действиями витапроста.
Пациентов, неудовлетворенных промежуточным (3 визит) и окончательным результатами (5 визит) лечения, не было (табл. 3). Число пациентов, отмечавших хороший и удовлетворительный результат терапии, прогрессивно увеличилось к окончанию исследования.
Нежелательных явлений, самостоятельно отмечаемых пациентами или диагностируемых объективно во время контрольных визитов, не наблюдалось. Случаев отмены препарата не было. Специальные исследования по оценке безопасности (физикальные исследования, клинические – анализ крови и мочи) не выявили клинически значимых отклонений от нормальных и исходных параметров после курса приема исследуемого препарата.
Заключение. Использованная нами схема терапии больных хроническим простатитом, сопровождающимся нарушениями сперматогенеза: витапрост в форме суппозиториев ректальных 50 мг по 1 суппозиторию 1 раз в сутки в течение 30 дней с последующим приемом витапроста в форме таблеток 100 мг внутрь, по 1 таблетке 2 раза в день в течение 40 дней – продемонстрировала свою эффективность, безопасность, хорошую переносимость и может быть рекомендована к применению.



