Введение. В эпоху развитой медицины, когда с онкологическими процессами в организме пытаются бороться путем химио- и лучевой терапии, малоинвазивными хирургическими методами, существуют ситуации, когда в опухолевый процесс вовлечены одновременно несколько органов малого таза: мочевые пути, женские гениталии и прямая кишка, при этом возникает необходимость в выполнении расширенных операций вплоть до тотальной тазовой экзентерации с формированием различных вариантов отведения мочи и кишечного содержимого [1].
История экзентерации таза берет начало с 1940 г., когда E. M. Bricker впервые выполнил эту операцию пациенту с мышечно-инвазивным раком мочевого пузыря [2].
О тазовой экзентерации по поводу местнораспространенного рака шейки матки впервые сообщил А. Brunschwig в 1948 г. [3], а в 1950 г. L. U. Appleby впервые сообщил о эвисцераци таза у 6 больных местнораспространенным раком прямой кишки [4].
До 1983 г. в мировой практике было произведено немногим более 200 экзентераций таза, а до 2004 г. в зарубежной литературе описано около 800 подобных операций. В настоящее время число таких операций неуклонно растет, что связано прежде всего с совершенствованием хирургической техники, развитием новых медицинских технологий и значительным ростом заболеваемости злокачественными опухолями органов малого таза во всем мире [5].
 Поскольку экзентерация органов малого таза сопровождается деривацией мочи и кишечного содержимого, такой фактор, как качество жизни после операции, должен рассматриваться хирургом наравне с послеоперационными осложнениями, общей и безрецидивной выживаемостью, а также летальностью [6].
Поскольку экзентерация органов малого таза сопровождается деривацией мочи и кишечного содержимого, такой фактор, как качество жизни после операции, должен рассматриваться хирургом наравне с послеоперационными осложнениями, общей и безрецидивной выживаемостью, а также летальностью [6].
Основным методом оценки качества жизни после экзентерации таза является анкетирование с помощью специальных опросников. Данные опросники должны включать следующие аспекты: послеоперационные проблемы, связанные с отведением мочи, сексуальную функцию и брак, профессиональную, социальную деятельность и работу по дому, настроение и эмоции [7]. В настоящее время утверждено несколько анкет для оценки качества жизни после экзентерации органов малого таза: FACT-G, EORTC QLQ-C30, EORTC QLQ-BLM, SF-36.
Представляем наш опыт выполнения передней экзентерации органов малого таза и результаты сравнения качества жизни пациенток после различных видов кишечной деривации мочи.
Материалы и методы. В ретроспективное исследование включены 60 женщин, которым в период с 2004 по 2014 г. в клинике урологии ГКБ им С. П. Боткина, РМАПО, выполнялась передняя экзентерация таза с различными способами деривации мочи. Средний возраст пациенток составил 53,2±3 (32–68) года.
По поводу рака мочевого пузыря передняя экзентерация таза выполнена 38 пациенткам. Рак мочевого пузыря стадии pT1N0M0 G3 диагностирован у 4 пациенток, pT2aN0M0 – у 8, pT2bN0M0 – у 12, pT3aN0M0 – у 7, pT3bN0M0 – у 4, pT4N0M0 – у 3.
Двадцати двум пациенткам передняя экзентерация таза выполнена по поводу постлучевых повреждений мочевыводящих путей: сложных постлучевых пузырно-влагалищных свищей с потерей емкости мочевого пузыря (микроцистис), комбинированных свищей (пузырно-мочеточниково-влагалищные, пузырно-влагалищно-прямокишечные).
 Для оценки качества жизни после передней экзентерации таза с различными видами деривации мочи пациентки были разделены на 3 группы. В 1-й 39 (65%) пациенткам выполнена инконтинентная деривация мочи (операция Bricker), во 2-й группе у 19 (31,66%) пациенток был сформирован ортотопический кишечный резервуар (операция Studer), в 3-й группе 2 (3,34%) пациенткам выполнена гетеротопическая деривация мочи с формированием катетеризируемого резервуара.
Для оценки качества жизни после передней экзентерации таза с различными видами деривации мочи пациентки были разделены на 3 группы. В 1-й 39 (65%) пациенткам выполнена инконтинентная деривация мочи (операция Bricker), во 2-й группе у 19 (31,66%) пациенток был сформирован ортотопический кишечный резервуар (операция Studer), в 3-й группе 2 (3,34%) пациенткам выполнена гетеротопическая деривация мочи с формированием катетеризируемого резервуара.
Качество жизни оценивали с помощью анкеты SF-36.
Результаты. Период наблюдения составил от 2 до 10 лет (медиана наблюдения – 5,6 года). В 1-й группе средняя продолжительность операции составила 4 (2–6) ч, средняя кровопотеря – 600 (500–1000) мл, во 2-й и 3-й группах в связи с формированием детубуляризированных резервуаров низкого давления средняя продолжительность операции составила 5 (2–7) ч, средняя кровопотеря – 700 (500–1200) мл.
Независимо от метода деривации мочи послеоперационная летальность составила 3%, 5-летняя общая выживаемость – 60,9±15,8% и 5-летняя безрецидивная выживаемость – 55,4±12,6%. В нашем исследовании мы также оценивали дневное и ночное удержание мочи при формировании резервуаров низкого давления, при этом ночное удержание отметили 79% пациенток, дневное удержание – 88,9%.
В 1-й группе хорошее качество жизни после передней экзентерации таза отметили 64% пациенток, во 2-й – 81%, в 3-й – 100%.
Итак, нами установлено, что качество жизни пациенток, перенесших ортотопическую деривацию мочи, выше, чем у пациенток после формирования инконтинентного илеокондуита. Все прооперированные с катетеризируемым резервуаром указали на хорошее качество жизни, однако сравнивать качество жизни пациенток с катетеризируемым резервуаром и пациенток, у которых сформирован ортотопический неопузырь, затруднительно в связи с небольшим числом наблюдений больных с гетеротопическим катетеризируемым резервуаром.
Приводим клинические наблюдения.
 1. Пациентка М. 38 лет в феврале 2015 г. находилась в нашей клинике с диагнозом: рак шейки матки рT1bN0M0. Состояние после расширенной экстирпации матки с транспозицией придатков матки от 27.02.10, дистанционной и внутриполостной лучевой терапии. Постлучевой рецидивный пузырно-влагалищный свищ. Микроцистис.
1. Пациентка М. 38 лет в феврале 2015 г. находилась в нашей клинике с диагнозом: рак шейки матки рT1bN0M0. Состояние после расширенной экстирпации матки с транспозицией придатков матки от 27.02.10, дистанционной и внутриполостной лучевой терапии. Постлучевой рецидивный пузырно-влагалищный свищ. Микроцистис.
С учетом наличия рецидивного пузырно-влагалищного свища, молодого возраста, объема поражения влагалища и мочевого пузыря, наличия микроцистиса, отсутствия технической возможности выполнить реконструктивную операцию по восстановлению мочеиспускания естественным путем пациентке 09.02.15 выполнена операция: цистэктомия, формирование гетеротопического континентного резервуара по Mainz pouch I с созданием удерживающего механизма по принципу Монти.
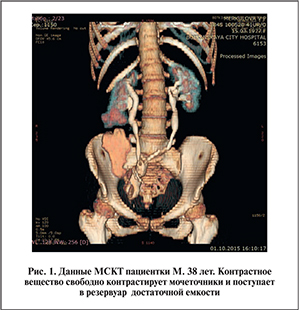
При контрольном УЗИ нарушения уродинамики верхних мочевых путей нет, резервуар дренируется адекватно. За время наблюдения эпизодов атак пиелонефрита не было. Пациентка обучена аутокатетеризации резервуара. По данным мультиспиральной КТ (МСКТ) контрастное вещество свободно контрастирует мочеточники и поступает в резервуар достаточной емкости (рис. 1). В удовлетворительном состоянии пациентка выписана. В настоящее время социально адаптирована, ведет активный образ жизни, занимается спортом (рис. 2).
2. Пациентка Б. 36 лет в феврале 2011 г. находилась в нашей клинике с диагнозом: рак шейки матки T3bNxM0, влагалищный и двусторонний параметральный вариант. Состояние после сочетанной лучевой и химиотерапии. Лучевой фиброз малого таза. Лучевой цистит. Лучевой эпителиит влагалища. Постлучевой пузырно-влагалищный свищ. Стриктура нижней трети правого мочеточника. Нефростома справа.
Выполнить реконструктивную операцию с использованием мягких тканей в имеющихся условиях не представлялось возможным. 06.03.11 пациентке проведена передняя экзентерация таза, операция Studer. При контрольном УЗИ нарушений уродинамики нет. В удовлетворительном состоянии пациентка выписана. Больная осуществляет мочеиспускание естественным путем. За время наблюдения атак пиелонефрита не было. По данным контрольной МСКТ контрастное вещество свободно контрастирует мочеточники и поступает в резервуар (рис. 3).
 В настоящее время пациентка социально адаптирована, работает менеджером в авиакомпании.
В настоящее время пациентка социально адаптирована, работает менеджером в авиакомпании.
3. Пациентка Д. 56 лет в марте 2009 г. находилась в нашей клинике с диагнозом: рак мочевого пузыря рT2bN1M0. Трансуретральная резекция стенки мочевого пузыря с опухолью от 20.02.09. Уретерогидронефроз справа. ХПН. Нефростома справа.
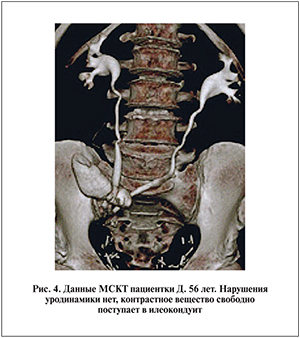
С учетом наличия мышечно-инвазивного рака мочевого пузыря, ХПН пациентке 11.03.15 выполнена передняя экзентерация таза, инконтинентная деривация мочи, операция Bricker. При контрольном УЗИ нарушения уродинамики не выявлено. Уростома функционирует удовлетворительно. За время наблюдения атак пиелонефрита не было. Пациентка в удовлетворительном состоянии выписана. По данным контрольной МСКТ нарушений уродинамики нет, контрастное вещество свободно поступает в илеокондуит (рис. 4).
Пациентка по данным опросника SF-36 отмечает удовлетворительное качество жизни, занимается домохозяйством.
Обсуждение. Статистические данные ВОЗ на конец 2010 г. свидетельствуют о том, что показатели заболеваемости раком прямой кишки, мочевого пузыря, шейки и тела матки составили 40,16 на 100 тыс. женщин и 27,01 на 100 тыс. мужского населения [8]. Именно эти локализации являются основными при местнораспространенных опухолях органов малого таза [Чиссов В. И. и др., 2012]. Заболеваемость новообразованиями внутренних половых органов у женщин в России также характеризовалась стабильным ростом. Общий прирост показателя заболеваемости за 10 лет (2000–2010) составил 25,76% при раке тела матки и 24,92% при раке шейки матки [8]. Заболеваемость новообразованиями мочевого пузыря в России также имеет выраженную тенденцию к росту. За 10 лет (2000–2010) общий прирост показателя заболеваемости составил 6,42% среди мужчин и 18,47% среди женщин. Уровни заболеваемости достигли в 2010 г. 1,96 у женщин и 12,46 – у мужчин на 100 тыс. населения [Чиссов В. И. и др., 2012].
В настоящее время экзентерацию органов малого таза в зависимости от объема удаляемых тканей принято разделять на переднюю (удаление мочевого пузыря, матки, влагалища), заднюю (удаление прямой кишки, матки, влагалища) и тотальную (удаление всех вышеперечисленных органов) [9].
Основные показания к выполнению экзентерации органов малого таза [10]:
- мышечно-инвазивный рак мочевого пузыря Т2, местнораспространенный рак стадии Т3–Т4, рак in situ, резистентный к лечению БЦЖ-терапией, частое рецидивирование поверхностного рака мочевого пузыря со снижением степени клеточной дифференцировки, безуспешность консервативного лечения;
- непрекращающаяся гематурия;
- местнораспространенный рак женской уретры, вульвы, влагалища;
- рак тела и шейки матки стадии Т3–Т4, рецидивирующий рак тела и шейки матки;
- сложные постлучевые пузырно-влагалищные свищи с потерей емкости мочевого пузыря (микроцистис), комбинированные свищи (пузырно-мочеточниково-влагалищные, пузырно-влагалищно-прямокишечные);
- местнораспространенный колоректальный рак.
Несмотря на практически 70-летнюю историю применения, отношение к тазовой экзентерации до настоящего времени остается неоднозначным.
К основным причинам непопулярности данной операции относятся [11]:
- техническая сложность и длительность операции;
- высокая частота интра- и послеоперационных осложнений (до 60%);
- послеоперационная летальность (до 30%);
- низкое качество жизни после операции;
- трудность реабилитации.
В настоящее время благодаря развитию хирургической техники, медицинских технологий и фармакологии доля экзентераций таза выросла, а вместе с этим снизилась частота послеоперационных осложнений и летальности, выросла общая выживаемость [12]. По данным литературы [5, 9, 10–12], послеоперационная летальность колеблется от 2 до 4%, 5-летняя общая выживаемость – 36–66%, что сопоставимо с полученными нами данными.
Так как экзентерация таза завершается отведением мочи или кишечного содержимого, сохранение удовлетворительного качества жизни остается одной из основных задач при выборе метода оперативного лечения [13]. Как указывалось выше, качество жизни оперированных нами пациенток оценивалось по-разному. Наилучшим оно оказалось для пациенток после континентной деривации мочи (100%), наихудшим – при формировании «влажной» илеостомы (64%).
Интересным представляется проведенный в 2015 г. наиболее крупный сравнительный мета-анализ качества жизни пациентов после ортотопической и кондуитной деривации мочи, в который вошло 21 исследование (2285 пациентов). При этом в 16 исследованиях пациенты не отметили никакой разницы в качестве жизни в зависимости от типов отведения мочи, в 4 сообщалось о лучшем качестве жизни у пациентов с ортотопическим неопузырем, в 1 исследовании лучшее качество жизни констатировали у пациентов с илеокондуитом [14]. По нашему мнению, до настоящего времени нет однозначных сравнительных исследований, демонстрирующих преимущества в качестве жизни для пациентов с ортотопической и кондуитной деривацией мочи, что требует проведения более крупных сравнительных исследований.
Выводы
- Несмотря на сложность техники выполнения, высокий риск послеоперационных осложнений и летальности, передняя экзентерация органов малого таза обеспечивает 5-летнюю общую выживаемость до 61% и 5-летнюю безрецидивную выживаемость до 56%.
- При местнораспространенных опухолях органов малого таза передняя экзентерация является спасительной операцией и позволяет сохранить удовлетворительное качество жизни.
- Для обеспечения удовлетворительного качества жизни и социальной адаптации у пациенток с инвазивным раком мочевого пузыря при соблюдении онкологических принципов методом деривации мочи является ортотопическая кишечная пластика.
- Методом деривации мочи после передней экзентерации таза у пациенток с постлучевыми повреждениями мочевыводящих путей является операция Брикера, в определенных ситуациях возможно формирование гетеротопических катетеризируемых резервуаров.



