Введение. В настоящее время основным способом надпузырной кишечной деривации мочи после цистэктомии является ортотопическая, или континентная, гетеротопическая цистопластика, которая обеспечивает лучшее качество жизни больных. Значительно реже выполняют илеокондуит по Бриккеру или билатеральный уретеросигмоанастомоз. Одним из отдаленных осложнений этих вмешательств являются камни мочевых путей, которые могут образовываться в самом резервуаре или верхних мочевыводящих путях (ВМП) в различные сроки после операции [1–3]. Высокий риск камнеобразования у этих больных связывают с анатомическими изменениями и метаболическими нарушениями [2–4]. При рефлюксирующих уретероилеальных анастомозах или их стриктурах постоянный стаз мочи на фоне нарушения уродинамики ВМП способствует образованию камней. У больных с континентными мочевыми резервуарами увеличивается экскреция кальция, фосфора и магния с мочой, что может быть причиной формирования камней [4, 5]. Кроме того, реабсорбция аммония из мочи через стенку кишки артифициального мочевого пузыря обусловливает увеличение кислотности мочи и повышение риска камнеобразования.
 У пациентов с кишечной деривацией мочи опасность формирования камней увеличивается из-за ее инфицированности [4–6]. Инфекция, поддерживаемая уреазапродуцирующими микроорганизмами, сопровождается образованием аммония в моче.
У пациентов с кишечной деривацией мочи опасность формирования камней увеличивается из-за ее инфицированности [4–6]. Инфекция, поддерживаемая уреазапродуцирующими микроорганизмами, сопровождается образованием аммония в моче.
В результате изменения ее кислотности повышается риск образования фосфата кальция и струвитных камней. Причем в этих случаях превалирует фосфат кальция, так как является первой солью, которая кристаллизируется при достижении pH мочи 6, тогда как струвитные камни образуются при pH мочи свыше 7.
При камнях ВМП в отношении больных после деривации мочи используются все имеющиеся на сегодняшний день методы дистанционной и контактной литотрипсии [7–10]. Дистанционная и трансуретральная пиелолитотрипсии по сравнению с перкутанной нефролитотрипсией (ПНЛ) являются менее инвазивными вмешательствами. Однако измененная анатомия мочевых путей у больных с кишечной деривацией мочи часто делает выполнение этих операций менее результативным или технически невозможным. При значительной плотности камня эффективность его дистанционного разрушения низкая, а вероятность обструкции мочеточника осколками высокая. Трансуретральный доступ не всегда возможен ввиду плохой визуализации в резервуаре устья мочеточника [8–10]. Таким образом, методом выбора при оперативном лечении крупных камней почки у этих больных является ПНЛ.
Материалы и методы. С 2001 по 2015 г. в нашей клинике 16 больным, перенесшим ранее различные способы деривации мочи (основная группа), выполнена ПНЛ по поводу крупных камней ВМП. Мужчин было 10 (62,5%), женщин – 6 (37,5%). Средний возраст больных составил 46,5±14,6 (от 26 до 74) года. Одиночные конкременты лоханки выявлены у 11 пациентов, множественные – у 2, камни мочеточника – у 2. У 1 больной имели место крупные камни гетеротопического резервуара и лоханки левой почки. Средний размер камней был 2,5 (2,2–3,6) см. Ранее 2 (12,5%) больным в связи с экстрофией мочевого пузыря был выполнен билатеральный уретеросигмоанастомоз, радикальная цистэктомия с ортотопической илеоцистопластикой произведена 12 (75%), гетеротопическая цистопластика – 2 (12,5%) пациентам. Показанием к деривации мочи в 2 случаях была экстрофия мочевого пузыря, в 12 – рак мочевого пузыря и в 2 – микроцистис. Сроки образования камней почек и мочеточника колебались от 10 мес до 3,6 года (в среднем 22 мес).
Контрольную группу составили 30 больных с крупными камнями почечной лоханки без кишечной деривации мочи, которым также была выполнена ПНЛ. Мужчин было 19 (63,3%), женщин – 11 (36,3%). Средний возраст больных составил 44,8±16,2 (от 30 до 70) года, средний размер камней – 2,6 (2,4–3,8) см.
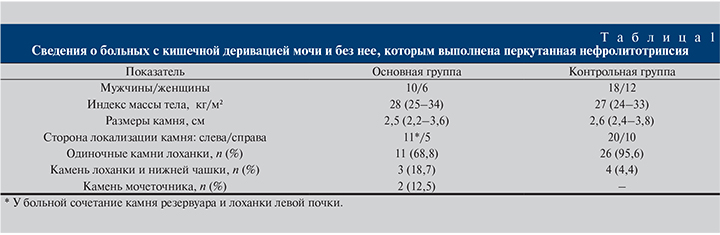
Характеристика больных обеих групп приведена в табл. 1.
Диагностика нефролитиаза основывалась на жалобах, данных анамнеза, результатах лабораторных и инструментальных методов обследования. Кроме ультразвукового исследования почек и экскреторной урографии всем больным выполнялась спиральная компьютерная томография. Эти методы позволили уточнить размер и плотность камня, его стереометрическое расположение, морфофункциональное состояние почек и ВМП. О функции почек судили на основании результатов динамической сцинтиграфии. Учитывая наличие хронической инфекции ВМП у больных основной группы, до операции им проводилась антибактериальная терапия.

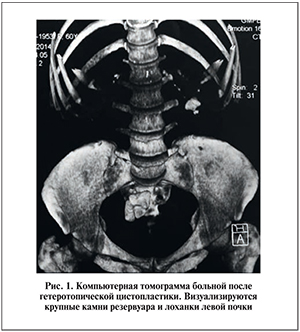
Всем больным ПНЛ выполняли в положении на животе. Пациентам с кишечной деривацией мочи предварительное внутривенное контрастирование чашечно-лоханочной системы (ЧЛС) не проводилось. Пункцию полостной системы почки выполняли под ультразвуковым контролем, а дилатацию пункционного хода до 26 Шр осуществляли под рентгенологическим контролем с использованием бужей Amplatz. Для нефроскопии использовали эндоскоп 22 Шр. После удаления сгустков крови и осмотра полостной системы почки проводили контактное дробление камня ультразвуковым литотриптером. Двум больным с камнями левого мочеточника выполнена антеградная лазерная уретеролитотрипсия. В одном наблюдении симультанно открытым доступом удалены камни из гетеротопического резервуара, а затем в положении на животе произведена ПНЛ слева (рис. 1, 2).
Больным контрольной группы вначале выполняли цистоскопию с катетеризацией мочеточника. Затем их укладывали на живот. Как и в основной группе, пункцию ЧЛС осуществляли под ультразвуковым контролем, а после бужирования нефростомического хода устанавливали кожух Amplatz. Во всех случаях после удаления камней осуществляли дренирование полостной системы почки нефростомическим катетером Фолея.

C целью оценки достоверности полученных цифровых показателей проводилась их статистическая обработка с использованием пакета программ Statistica 6,0 for Windows, Microsoft Excel. Анализ достоверности различия средних величин проведен по критерию Стьюдента (t-критерия). Статистически значимыми считались результаты при значении p<0,05.
Результаты. Геморрагических осложнений, потребовавших проведения гемотрансфузии, не возникло ни у одного больного. Обострение хронического пиелонефрита имело место у 4 (25%) больных основной группы и у 3 (10%) – контрольной. Перкутанная нефролитотрипсия в качестве монотерапии была эффективной в отношении 14 (87,5%) из 16 больных с деривацией мочи и 27 (90%) из 30 пациентов контрольной группы (табл. 2). По данным динамической сцинтиграфии у всех пациентов отмечали нормализацию уродинамики ВМП и улучшение функции почки.
Приводим клиническое наблюдение успешной ПНЛ камня единственной левой почки у больного, которому в детстве был выполнен билатеральный уретеросигмоанастомоз по поводу экстрофии мочевого пузыря.
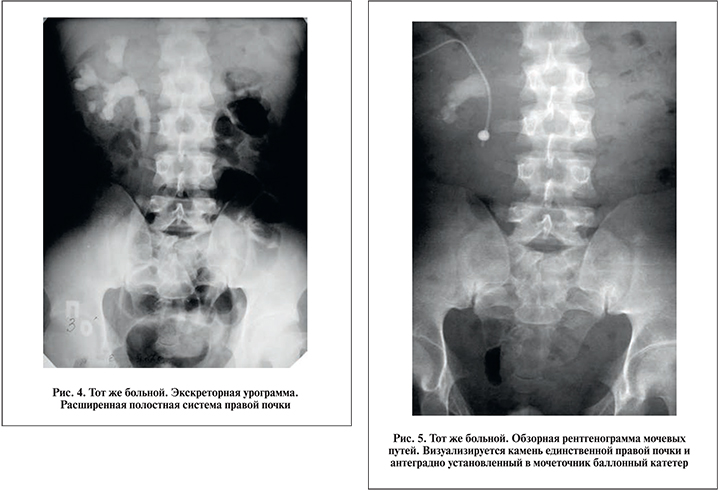
Б о л ь н о й 26 лет госпитализирован в нашу клинику 15.10.2009 с жалобами на боли в правой поясничной области и лихорадку до 39 ˚С с ознобами. По данным ультразвукового исследования и экскреторной урографии выявлен камень единственной правой почки, расширение ее полостной системы (рис. 3, 4). Из анамнеза известно, что в 1986 г. был выполнен билатеральный уретеросигмоанастомоз в связи с экстрофией мочевого пузыря, а в 1996 г. по поводу пионефроза удалена левая почка. Учитывая наличие обструктивного пиелонефрита, 16.10.2009 выполнена чрескожная пункционная нефростомия справа. При пункции получена моча со зловонным запахом и большим количеством слизи вследствие рефлюкса кишечного содержимого в ВМП. В посеве мочи выявлен рост E. сoli в титре 106 КОЕ/мл. Проведенная антибактериальная терапия и дренирование полостной системы почки не дали значительного клинического эффекта. Сохранялась фебрильная температура, в анализах крови отмечался высокий лейкоцитоз со сдвигом формулы влево.
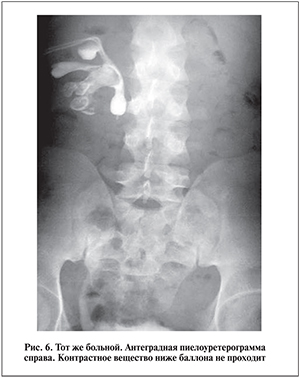 С целью устранения поступления кишечного содержимого в почку в верхнюю треть мочеточника перкутанным доступом был установлен баллонный катетер. По данным обзорной рентгенографии мочевых путей и антеградной пиелографии баллон плотно обтурировал просвет мочеточника, контрастное вещество ниже его не поступало (рис. 5, 6). Такая тактика позволила ликвидировать рефлюкс кишечного содержимого в полостную систему почки и купировать обострение хронического пиелонефрита. В дальнейшем больному выполнена ПНЛ справа. Послеоперационных осложнений не было. Баллонный катетер удален через 2 нед. В настоящее время состояние больного удовлетворительное. Учитывая молодой возраст пациента, постоянный кишечно-лоханочный рефлюкс справа и риск развития опухоли толстой кишки, ему выполнена гетеротопическая илеоцистопластика.
С целью устранения поступления кишечного содержимого в почку в верхнюю треть мочеточника перкутанным доступом был установлен баллонный катетер. По данным обзорной рентгенографии мочевых путей и антеградной пиелографии баллон плотно обтурировал просвет мочеточника, контрастное вещество ниже его не поступало (рис. 5, 6). Такая тактика позволила ликвидировать рефлюкс кишечного содержимого в полостную систему почки и купировать обострение хронического пиелонефрита. В дальнейшем больному выполнена ПНЛ справа. Послеоперационных осложнений не было. Баллонный катетер удален через 2 нед. В настоящее время состояние больного удовлетворительное. Учитывая молодой возраст пациента, постоянный кишечно-лоханочный рефлюкс справа и риск развития опухоли толстой кишки, ему выполнена гетеротопическая илеоцистопластика.
Особенность данного клинического наблюдения заключается в том, что у больного кроме камня единственной правой почки наблюдался кишечно-лоханочный рефлюкс, поддерживающий постоянный воспалительный процесс в ВМП. Обтурация мочеточника баллонным катетером позволила предотвратить заброс кишечного содержимого в лоханку, провести антибактериальную терапию, а затем и ПНЛ.
Обсуждение. Камнеобразование в мочевых путях является одним из отдаленных осложнений кишечной деривации мочи. Так, по данным литературы, в 12% случаев после тонкокишечной цистопластики и в 4% – после толстокишечной деривации мочи наблюдаются камни почек (чаще струвитные) [6]. Причиной образования камней у этих больных являются различные метаболические и анатомические изменения [2–5].
Выбор метода лечения камней ВМП для больных с кишечной деривацией мочи зависит от различных факторов, таких как размер камня, его локализация и строение ЧЛС. Дистанционная литотрипсия показана при небольших камнях низкой плотности, а ее эффективность, по данным [7], достигает 81,5%. При подобных камнях ВМП можно выполнить контактную уретеролитотрипсию, но ретроградный доступ является сложным или не всегда технически возможным. F. Delvecchio и соавт. [8] рекомендуют использовать комбинацию антеградного и ретроградного доступов.
Альтернативным методом лечения крупных камней почек у больных после различных способов деривации мочи является ПНЛ [9, 10]. Данная операция обеспечивает высокий процент освобождения от камней с минимальными осложнениями, но требует достаточного опыта в создании чрескожного пункционного доступа в почку или перкутанной хирургии нефролитиаза. Одним из немаловажных технических моментов ПНЛ является обеспечение доступа в мочеточник для ретроградного контрастирования полостной системы почки. Идентификация устья мочеточника и установка катетера могут быть технически сложными для большинства пациентов с кишечной деривацией мочи. При рефлюксирующих мочеточниково-кишечных анастомозах тугое заполнение резервуара приводит к ретроградному контрастированию ВМП, что сравнительно облегчает пункцию ЧЛС. Однако резкое повышение интраренального давления может стать причиной пиеловенозного рефлюкса и бактериотоксического шока. В некоторых случаях используется интравенозное контрастирование или прямая пункция ЧЛС с антеградным введением контрастного вещества. При достаточном опыте в перкутанной ренальной хирургии полостную систему почки пунктируют под ультразвуковым наведением, а затем проводят дилатацию нефростомического хода под рентгенологическим контролем. При одиночных камнях лоханки ПНЛ можно выполнить только под ультразвуковым контролем [11–14].
В литературе мало публикаций о результатах ПНЛ у больных с кишечной деривацией мочи. A. Fernandez и соавт. [10] выполнили ПНЛ 30 подобным больным, а полученные результаты сравнили с контрольной группой из 100 больных. Инфекция ВМП в группе с деривацией мочи (64%) встречалась значимо чаще, чем в контрольной (15%). Время операции у больных с деривацией мочи составило 83±42,2 мин, в контрольной – 84,2±36,5 мин. Эффективность ПНЛ составила 76 и 83% соответственно. Такие невысокие показатели, видимо, связаны с тем, что в первой группе 40% больных имели рецидивные камни, во второй – 48%. В нашей серии эффективность ПНЛ в группе больных с деривацией составила 87,5%, в контрольной группе – 90% в отсутствие статистически значимых различий. Также не различались продолжительность ПНЛ, объем интраоперационной кровопотери и сроки госпитализации.
У больных с кишечной деривацией мочи имеет место постоянная хроническая инфекция ВМП, что может быть причиной развития инфекционных осложнений при ПНЛ. Высокий риск послеоперационной инфекции и сепсиса заставляют вносить определенные коррективы в предоперационную подготовку подобных больных, которая в основном заключается в проведении антибактериальной терапии и назначении лекарств, улучшающих почечную гемодинамику. Однако, несмотря на предоперационную подготовку, у 4 (25%) больных основной группы наблюдалось обострение хронического пиелонефрита, что оказалось достоверно чаще, чем в контрольной группе (10%). Данный факт указывает на необходимость адекватной предоперационной санации ВМП.
Заключение. Таким образом, лечение больных с кишечной деривацией мочи из-за нарушения анатомии ВМП для эндоурологов сопряжено с техническими сложностями. У подобной категории больных ввиду низкой эффективности дистанционной литотрипсии и невозможности выполнения трансуретральной уретероскопии оптимальна ПНЛ. Она позволяет с минимальными осложнениями и высокой эффективностью удалять крупные камни почек у больных, перенесших различные методы отведения мочи.


