Введение. Хронический простатит – широко распространенное, трудноизлечимое заболевание, отношение к которому у врачей и их пациентов остается неоднозначным. К одним из факторов, определяющих трудность диагностики и лечения данного состояния, относится полиморфность клинической картины. Типичными проявлениями хронического простатита считаются боль в малом тазу, нарушения мочеиспускания, а также разнообразная астеновегетативная симптоматика [1, 2]. Немаловажное влияние на качество жизни пациентов с хроническим простатитом могут оказывать расстройства копулятивного цикла, а именно его эректильного и эякуляторного компонентов [3, 4].
Воспаление предстательной железы любого генеза может распространяться на соседние анатомические структуры, например на сосудисто-нервные пучки, проходящие в непосредственной близости от этого органа [1, 5]. Согласно классическим постулатам патологической физиологии, существует пять местных признаков воспаления: припухлость, покраснение, повышение температуры, боль и потеря функции [6]. Именно нарушение функции нервных волокон и кровеносных сосудов, направляющихся к половому члену, может стать пусковым моментом в развитии эректильной дисфункции [7, 8]. При психической астенизации пациента эректильную дисфункцию дополнительно усугубляет снижение либидо [5].
Нарушение иннервации гениталий приводит также к снижению порога эякуляторного рефлекса, что проявляется преждевременной эякуляцией. Этому способствует и поражение семявыбрасывающих протоков, анатомически расположенных в толще предстательной железы [9, 10]. Простата, семенные пузырьки и протоковая система непосредственно участвуют в акте эякуляции, поэтому воспалительные процессы, локализованные в простатовезикулярном комплексе, могут сопровождаться болью в промежности при семяизвержении и стертостью оргастических ощущений [3, 9, 11].

Хорошо известно, что нарушения эрекции и эякуляции усугубляют друг друга посредством таких психологических механизмов, как снижение либидо и формирование синдрома ожидания сексуальной неудачи [4]. Физиологической основой этого феномена может быть избыточная адренергическая (симпатическая) активность, снижающая порог эякуляторного рефлекса и неблагоприятным образом влияющая на эректильный рефлекс, который по своей природе является парасимпатическим [12].
Подобные копулятивные дисфункции могут провоцировать отказ от половой жизни, а в некоторых случаях – и от суррогатной половой активности. Это усугубляет гемодинамические нарушения в области малого таза и конгестию в ацинарно-протоковой системе предстательной железы [1]. Налицо формирование многоуровневого порочного круга в патофизиологии хронического простатита с ассоциированной эректильной и эякуляторной дисфункциями [4]. Данные патогенетические взаимоотношения могут быть отражены схематически (см. рисунок).
Практически все хронические заболевания имеют в своем патогенезе несколько взаимоусугубляющих факторов, что и определяет трудности в их лечении. Патогенетическая терапия позволяет надеяться на успех только в том случае, если терапевтические факторы направлены на прерывание причинно-следственных отношений, формирующих порочный круг [13, 14]. Не является исключением и хрониче- ский простатит. При простатите целесообразно применение препаратов, мишенью которых служит не только воспалительный процесс, но и сексуальная дисфункция [15–17].

К одним из подобных препаратов относится простанорм, в состав которого входят экстракты солодки, золотарника, эхинацеи и зверобоя [18, 19].
Глицирризин, содержащийся в солодке, обладает противовоспалительным и гепатопротективным эффектами, немаловажными в условиях длительной агрессивной фармакотерапии хронического простатита [20].
Эноксолон, также экстрагируемый из корней солодки, имеет широкий спектр антимикробной активности, в который входят не только бактериальные и протозойные возбудители, но и вирусы [20].
Кверцетин, входящий в состав экстракта золотарника канадского, может применяться при метаболическом синдроме, а также имеет доказанный эффект в лечении синдрома хронической тазовой боли [21].
Эхинакозид и другие фенольные соединения эхинацеи пурпурной обладают антимикробными и антиоксидантными свойствами; будучи биологиче- скими стимуляторами, они способны опосредованно повышать общее самочувствие и либидо пациента [22].
Жирорастворимые алкиламиды эхинацеи обладают тропностью к CB2-разновидности каннабиноидных рецепторов, чем она и обязана своей репутации самого известного природного иммуномоду- лятора [22].
Содержащиеся в зверобое гиперфорин и гиперицин помимо антибактериальных свойств имеют способность блокировать обратный захват серотонина в головном мозге, благодаря чему являются природными антидепрессантами, а также задерживают эякуляторный рефлекс и продлевают время полового акта [23].
Благодаря вышеперечисленным свойствам компонентов простанорма представляется целесообразным его включение в схему комбинированной терапии хронического простатита, осложненного сексуальной дисфункцией.
Целью исследования стала оценка эффективности препарата простанорм в составе комбинированной терапии хронического простатита и сопутствующей копулятивной дисфункции.
Материалы и методы. В исследование включены 60 пациентов с диагнозом «хронический бактериальный простатит», подтвержденным при помощи микроскопического и бактериологического анализа секрета предстательной железы. Для всех пациентов возбудителем простатита служила условно-патогенная бактериальная флора: E. coli, E. faecalis, K. pneumoniae, P. aeruginosa (табл. 1). Диагностически значимым титром микроорганизмов считали 103 (КОЕ/мл) [24, 25]. У некоторых пациентов в секрете простаты обнаруживалось несколько микроорганизмов в диагностически значимом титре. Определяли чувствительность микрофлоры к антибактериальным препаратам. Возможные внутриклеточные возбудители (Chlamydia, Mycoplasma, Ureaplasma), а также протозойная (Trichomonas vaginalis) и вирусная (Herpes simplex) этиология простатита были исключены с помощью полимеразной цепной реакции.
В исследование включили пациентов с болью, локализованной в малом тазу, и эректильной дисфункцией, критерием которой служила сумма баллов менее 21 по системе Международного индекса эректильной функции (МИЭФ-5). Продолжительность сексуальных контактов, со слов пациентов, редко превышала 1 мин, что соответствует определению преждевременной эякуляции, данному Международным обществом сексуальной медицины (ISSM).
Пациенты были разделены на две сопоставимые группы по 30 человек. В контрольной группе пациенты получали стандартную антибактериальную терапию. В соответствии с рекомендациями Европейской ассоциации урологов в качестве антибактериального препарата был выбран левофлоксацин (per os, 500 мг, 1 раз в сутки, 28 дней) [25]. При бактериологическом исследовании секрета простаты с определением чувствительности микрофлоры к антибактериальным препаратам резистентных к левофлоксацину возбудителей не выявлено. Для профилактики кандидомикоза 1 раз в неделю назначали флуконазол в дозе 150 мг. Пациентам основной группы в схему лечения был добавлен простанорм по 2 таблетки 3 раза в день, продолжительность курса – 1 мес.
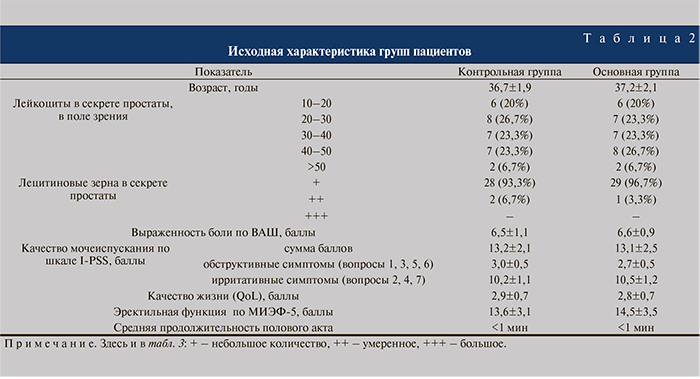
Выраженность воспалительного процесса и конгестии в предстательной железе оценивали по количеству лейкоцитов и лецитиновых зерен, обнаруженных при микроскопии секрета простаты. Проводили контрольное бактериологическое исследование секрета предстательной железы. Интенсивность боли оценивали с помощью визуальной аналоговой шкалы (ВАШ), качество мочеиспускания — по опроснику I-PSS, степень эректильной дисфункции – по опроснику МИЭФ-5. Со слов пациента оценивали также примерную продолжительность полового акта. На момент начала лечения группы были сопо- ставимы по возрасту и выраженности симптомов (табл. 2).
Оценку состояния проводили до лечения и на 30-й день после начала лечения.

Полученные показатели сравнивали с помощью статистического критерия Манна–Уитни и критерия согласия Пирсона.
Результаты. На момент контрольного обследования у 24 (80%) пациентов контрольной группы количество лейкоцитов в секрете простаты составило менее 10 в поле зрения при оптическом увеличении в 40 раз, что говорит о купировании воспалительного процесса (табл. 3). В основной группе подобные изменения были отмечены у 28 (93,3%) пациентов (p>0,05). Можно предположить, что простанорм в составе комбинированной терапии повышает ее эффективность, однако статистическое подтверждение этого тезиса требует проведения исследования с большим числом пациентов. Контрольное бактерио- логическое исследование секрета предстательной железы всех 60 пациентов, включенных в исследование, дало отрицательный результат.
В результате лечения у 29 (96,7%) пациентов, принимавших простанорм, при микроскопии секрета предстательной железы обнаружено значительное количество лецитиновых зерен, которые покрывали все поле зрения. В контрольной группе такие изменения, свидетельствующие о полном восстановлении функции простаты, наблюдались только у 14 (46,7%) пациентов. Умеренное количество лецитиновых зерен, свидетельствующее лишь о частичном восстановлении ее функции, регистрировали у 15 (50%) пациентов контрольной группы и лишь у 1 (3,3%) – основной (p<0,05).
Средний балл по ВАШ, характеризующий боль или дискомфорт в малом тазу, после окончания курса лечения составил 3,1 и 1,8 в контрольной и основной группах соответственно (p>0,05).
Сумма баллов по анкете I-PSS после курса лечения составила в среднем 7,9 в контрольной группе против 4,8 в основной (p<0,05). Следует отметить, что уменьшение суммарного балла I-PSS было обусловлено главным образом снижением интенсивности симптомов фазы накопления. Уменьшение выраженности ирритативной симптоматики было более выражено в группе пациентов, принимавших простанорм (p<0,05). Обструктивная симптоматика, оцениваемая по вопросам 1, 3, 5 и 6 анкеты I-PSS, изначально вносила относительно небольшой вклад в клиническую картину хронического простатита у наших пациентов и на фоне лечения существенно не изменялась. Динамика индекса QoL свидетельствовала об улучшении качества жизни после лечения, при этом разницы между группами пациентов выявлено не было (p>0,05).
Количество баллов по опроснику МИЭФ-5 в контрольной группе после стандартного курса лечения составило в среднем 21,2, в то время как при добавлении в терапевтическую схему простанорма – 24,3 (p<0,05). Средняя продолжительность полового акта увеличилась в среднем до 2,2 и 2,8 мин в контрольной и основной группах соответственно, однако данное различие оказалось статистически незначимым (p>0,05). Ни один из пациентов обеих групп по окончании лечения не предъявлял жалоб на боль при эякуляции.
Обсуждение. Как стандартная, так и дополненная простанормом схема лечения позволила эффективно купировать воспалительный процесс в предстательной железе. Однако устранение воспаления как такового не может считаться самостоятельной целью в лечении хронического простатита. Далеко не всегда оно приводит к восстановлению функции предстательной железы [3, 17, 26]. Иногда отсутствие воспалительных изменений в секрете простаты и вовсе обманчиво: оно может говорить о переходе инфекционно-воспалительного процесса в латентную фазу или о блокаде ацинарно-протоковой системы железы вязким секретом [1]. В группе пациентов, принимавших простанорм, чаще отмечалось увеличение количества лецитиновых зерен в секрете простаты, что говорит о восстановлении ее экзокринной функции и, следовательно, об истинном купировании воспаления.
Включение простанорма в курс лечения хрониче- ского простатита позволяет быстрее нормализовывать уродинамические параметры и устранять ирритативную симптоматику, что подтверждают данные, полученные в ходе нашего исследования. Кроме того, благодаря противовоспалительным и анальгетическим свойствам компонентов простанорма большей части пациентов удалось окончательно избавиться от вялотекущего синдрома хронической тазовой боли.
Копулятивные дисфункции, ассоциированные с хроническим простатитом, успешно поддаются коррекции с помощью препарата простанорм. Его включение в схему терапии позволяет нормализовывать эректильную функцию и увеличивать продолжительность полового акта этой категории пациентов, что существенно сказывается на общей эффективности лечения.
Примитивное понимание хронического простатита как рядового «воспалительного заболевания» служит источником неисчислимых врачебных ошибок [7]. Только комплексная терапия с воздействием на все звенья его патогенеза, в том числе и на нарушения копулятивного цикла, может считаться эффективной [15–17].



