Рецидивирующими инфекциями нижних мочевых путей в России страдают около 10% женщин. Основным методом лечения бактериальных инфекций, в том числе и ИМП, является антибактериальная терапия. Антибиотикорезистентность, которая традиционно считалась проблемой только для внутрибольничных и осложненных ИМП, выходит сейчас на первый план и при неосложненных амбулаторных ИМП [1]. За последние десятилетия в мире отмечено несколько тенденций в динамике антибиотикорезистентности уропатогенной E. coli, заставляющих пересматривать требования к выбору антибиотиков для терапии ИМП. Прежде всего это распространение штаммов, устойчивых к аминопенициллинам и ко-тримоксазолу, а в некоторых странах мира – и к фторхинолонам [2, 3].
В рекомендациях Европейской ассоциации урологов (EAU) по ведению больных инфекциями почек, мочевыводящих путей и мужских половых органов 2008 г. все исследования классифицированы в соответствии с уровнями доказательности данных, и каждая разработанная на их основе рекомендация отнесена в соответствующую категорию (табл. 1, 2) [4].
Будущее –за медициной не только предупредительной, но и доказательной. Любой теоретический постулат: прежде чем внедряться в рутинную практику, должен быть проверен и подтвержден данными клинических исследований и наблюдательных программ, определяющими уровень доказательности этого тезиса.
В настоящее время как отечественные, так и зарубежные рекомендации предлагают практикующим врачам для терапии рецидивирующих ИМП, во-первых, антибиотик, подобранный с учетом определения чувствительности возбудителя или с учетом данных о локальной резистентности возбудителей, эмпирически, во-вторых, препарат для профилактики, среди которых наивысший уровень рекомендаций имеют иммунотропные препараты [4, 5]. С учетом продолжающегося роста резистентности к фторхинолонам, с одной стороны, и современных эпидемиологических особенностей цистита, демонстрирующих расширение спектра возбудителей и изменение их антигенных свойств, с другой – сохраняется потребность в антибактериальном препарате, эффективном в отношении как E. coli, так и других наиболее частых этиологических агентов цистита, в том числе условнопатогенных.
С учетом результатов международного исследования ARESC (2003–2006), а также данных, полученных в российском исследовании ДАРМИС (2010–2011) [6], больным рецидивирующими инфекциями нижних мочевыводящих путей [5, 7, 8] рекомендуется применение полных курсов антибактериальной терапии препаратами фосфомицина трометамол, фуразидина калиевая соль с магния карбонатом, цефиксим, цефтибутен, левофлоксацин или ципрофлоксацин.

Чем у´же показания к применению антибиотика, тем дольше сохраняется чувствительность возбудителей к данному препарату. При этом неизменным требованием к антибиотику для лечения цистита является его безопасность, которая во многом определяется его фармакокинетикой, а именно способностью создавать избирательно высокие концентрации – в первую очередь в моче. Перечисленным требованиям соответствует цефалоспорин III поколения цефиксим (Супракс® Солютаб®, ранее Цефорал® Солютаб®, «Астеллас Фарма Юроп Б.В».) [9, 10]. Кроме того, при рецидивирующих ИМП, когда невозможно полностью избавиться от проблемы, задачей является увеличение безрецидивного периода путем проведения адекватной профилактики рецидивов. В настоящее время наибольшую доказательную базу в качестве средства профилактики рецидивов имеет представленный на российском рынке препарат Уро-Ваксом® – лиофилизированный лизат 18 штаммов уропатогенной E. coli (LE: 1a, GR: B) [11–14].
В целях анализа эффективности и безопасности препаратов цефиксим (Цефорал® Солютаб®) и Уро-Ваксом® при неосложненных рецидивирующих ИМП у женщин в рутинной клинической практике в России была проведена проспективная наблюдательная программа FLORA.
Материалы и методы. По дизайну исследование представляло проспективную наблюдательную программу и проводилось без какого-либо вмешательства в существующую терапевтическую практику врачей – участников исследования и полностью соответствовало общепринятым стратегиям лечения цистита, применяемым в клинических центрах. Работа выполнена в соответствии с этическими принципами проведения наблюдательных программ. Набор пациенток осуществлен в 5 центрах на территории Российской Федерации: Российской медицинской академии последипломного образования, Первом Московском государственном медицинском университете им. И. М. Сеченова, Московском государственном медико-стоматологическом университете им. А. И. Евдокимова, Красноярском государственном медицинском университете им. В. Ф. Войно-Ясенецкого, Ростовском государственном медицинском университете.
В программу включены пациентки, подписавшие информированное согласие на участие в данном исследовании, соответствующие критериям включения и исключения, с установленным диагнозом рецидивирующей ИМП, которым были назначены препараты Цефорал® Солютаб® и Уро-Ваксом®. План обследования, инструментальные методы диагностики и процедуры контроля эффективности лечения определены лечащим врачом в рамках рутинной практики лечебно-профилактических учреждений (ЛПУ) и в РФ.
Критерии включения в наблюдательную программу: наличие в анамнезе до включения в программу как минимум двух обострений рецидивирующих ИМП в течение 6 мес по данным истории болезни, наличие клинических признаков обострения ИМП как минимум в течение двух последних дней, наличие бактериурии ≥103 КОЕ/мл. Критерии исключения: продолжающаяся антимикробная профилактика или любая иммуностимулирующая терапия за 3 мес до включения в исследование.
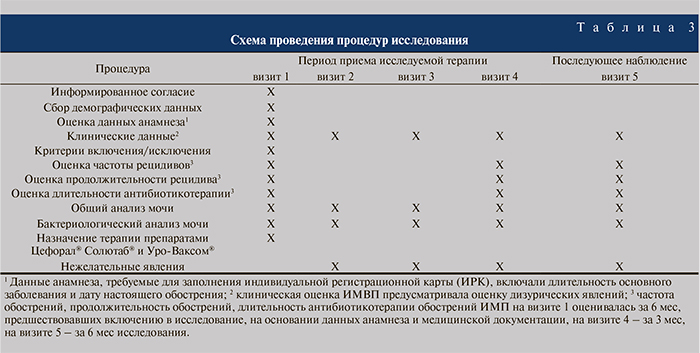
Каждая пациентка, за исключением выбывших преждевременно, в ходе программы выполнила 5 визитов к врачу (табл. 3).
Во время визита 1 врач-исследователь подписывал информированное согласие от пациентки на участие в программе, оценивал соответствие пациентки критериям включения/исключения, осуществлял сбор и фиксацию данных анамнеза, демографических данных, проводил оценку клинических проявлений и данных лабораторных обследований (общий анализ мочи, бактериологический анализ мочи), принимал решение о назначении терапии препаратами Цефорал® Солютаб® и Уро-Ваксом®. На визите 2 через 10±2 дня после визита 1 врач проводил оценку эффекта назначенной терапии, делал отметки об изменении режима терапии (если оно по какой-либо причине производилось), отмечал наличие нежелательных явлений. Визит 3 через 1 мес±1 неделя после визита 1 предусматривал оценку тех же параметров, что и на визите 2.
На визите 4 через 3 мес±2 нед после визита 1 наряду с обозначенными для визитов 2 и 3 параметров исследователь отмечал количество рецидивов ИМП за истекший 3-месячный период наблюдения и общую продолжительность рецидивов за данный период в днях, общую продолжительность лечения антибиотиками. Целью заключительного визита 5 через 6 мес±4 нед после визита 1 было оценить исходы назначенной терапии по параметрам, оцениваемым на визите 4, но за период 6-месячного наблюдения за пациенткой. В целом клинико-диагностические процедуры в рамках исследования проведены согласно существующей в центрах врачебной практике.
Оценка эффективности и безопасности терапии в рамках программы проведена по конечным точкам. Первичная конечная точка рассматривалась как частота обострений рецидивирующих ИМП на 1 пациентку через 6 мес с момента включения в программу (общее количество рецидивов ИМП по сравнению с исходным уровнем). Вторичными конечными точками были продолжительность обострений рецидивирующих ИМП на 1 пациентку через 6 мес с момента включения в программу по сравнению с исходным уровнем, продолжительность лечения антибиотиками обострений рецидивирующих ИМП на 1 пациентку через 6 мес после включения в программу по сравнению с исходным уровнем и частота нежелательных реакций.
Статистический анализ данных эффективности осуществлен в ITT (intent to treat)-популяции, т.е. среди всех пациенток, которые получили хотя бы одну дозу Цефорала® Солютаб® или Уро-Ваксома® в рамках исследования, при включении имели пригодные для оценки показатели и от которых был получен по крайней мере один результат оценки исхода лечения. Безопасность оценивали у всех пациенток, получавших в рамках исследования хотя бы одну дозу препаратов Цефорал® Солютаб® и/или Уро-Ваксом®. Для основных показателей были рассчитаны значения среднего, среднеквадратичного отклонений, медианы, квартилей.
Результаты. Информированное согласие на участие в исследование подписали 52 пациентки, составившие популяцию для оценки безопасности, а также клинико-демографических данных.
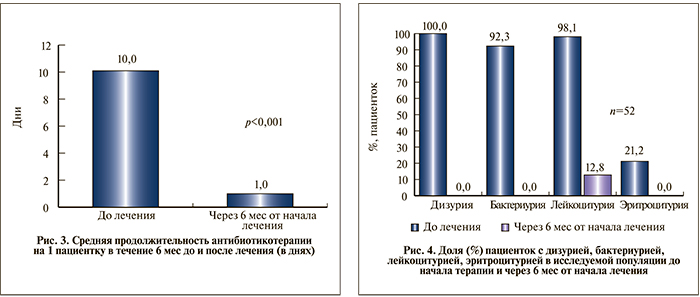
Клинико-демографические данные и информация о заболевании. Все включенные пациенты (n=52) были женского пола. Средний возраст пациенток составил 42,4±16,2 года, средняя продолжительность заболевания (цистита) – 1,1±2,6 года, в течение 6 мес до включения в исследование среднее количество рецидивов составило 2,9±1,0 и средняя длительность рецидива – 8,6±2,7 дня. В течение 6 мес, предшествовавших включению в исследование, среднее суммарное количество дней антибиотикотерапии составило 10,0±4,5 дня. Дизурические проявления на основании жалоб были отмечены у всех 52 (100%) пациенток. Согласно исходным показателям общего и бактериологического анализов мочи, у 51 (98,1%) пациентки имела место лейкоцитурия, у 11 (21,2%) – эритроцитурия, у 48 (92,3%) – бактериурия ≥103 КОЕ/мл.

Всем пациенткам, включенным в исследование, была назначена терапия препаратами Цефорал® Солютаб® и Уро-Ваксом®. Средняя продолжительность курса лечения препаратом Цефорал® Солютаб®, который назначали в дозе 400 мг 1 раз в день, составила 8,3±1,1 дня (доступны данные 51 пациентки, у одной пациентки дата окончания терапии не указана). Уро-Ваксом® был назначен на первом визите всем пациенткам в дозе 6 мг 1 раз в день, средняя продолжительность лечения составила 95,2±17,9 дня. Причины прекращения лечения препаратами представлены в табл. 4.
В ходе программы 5 пациенток получали сопутствующую терапию препаратами Фурамаг® – 1 (1,9%), доксициклин – 1 (1,9%), Вагинорм С® – 1 (1,9%), Экофемин® – 1 (1,9%), Везикар® – 1 (1,9%).
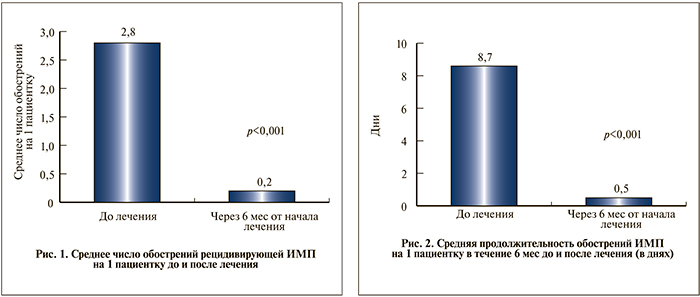
Оценка эффективности. В качестве первичной конечной точки анализировали частоту обострений рецидивирующих ИМП на 1 пациентку через 6 мес от момента включения в программу (общее количество рецидивов ИМП по сравнению с исходным уровнем, отмеченным за 6 мес, предшествовавших включению в программу). Среднее число рецидивов за 6 мес до включения и в течение 6 мес после включения в исследование представлено на рис. 1. Отмечено значимое снижение числа обострений в течение 6 мес (медиана разности числа обострений ИМП в течение 6 мес с момента включения и в течение 6 мес до включения статистически значимо [p<0,001] отличалась от 0 [критерий знаковых рангов Уилкоксона для связанных выборок]).
Вторичные конечные точки включали продолжительность обострений рецидивирующей ИМП на 1 пациентку через 6 мес с момента включения в программу по сравнению с исходным уровнем, а также продолжительность антимикробной терапии и число нежелательных явлений. Средняя продолжительность обострений рецидивирующих ИМП представлены на рис. 2. Изменение средней длительности обострений через 6 мес наблюдения по сравнению с исходным составило -8,0±3,0, изменение медианы – -8,0 [-10,0;-7,0], что значимо (p<0,001) отличалось от 0 (критерий знаковых рангов Уилкоксона для связанных выборок).
Средняя продолжительность лечения антибиотиками обострений рецидивирующей ИМП до включения в программу и через 6 мес после включения представлена на рис. 3. Изменение средней длительности антибиотикотерапии составило -9,3±5,0, медианы – -8,0 [-11,0; -7,0], что значимо (p<0,001) отличалось от 0 (критерий знаковых рангов Уилкоксона для связанных выборок).
На рис. 4 представлена динамика клинико-лабораторных показателей на фоне лечения.
Оценка безопасности. В процессе анализа безопасности ни у одной из пациенток, принявших хотя бы однократно препараты Цефорал® Солютаб® и/или Уро-Ваксом®, в ходе программы не было выявлено нежелательных явлений.
Обсуждение. Результаты, полученные в наблюдательной программе FLORA, позволяют сделать следующее заключение: режим терапии, включающий Цефорал® Солютаб® и Уро-Ваксом®, пациенток с рецидивирующей ИМП позволяет значительно снижать число рецидивов – через 6 мес у пациенток отмечено уменьшение среднего количества обострений на 93% по сравнению с исходным уровнем (2,8±1,0 против 0,2±0,4). В схожих исследованиях [15, 16] по оценке динамики числа рецидивов через 6 мес у пациенток, принимавших Уро-Ваксом® в течение 3 мес после стандартного курса антибиотикотерапии, продемонстрировано снижение количества обострений на 62–76%. Подобные различия могут быть связаны с тем, что эффективность режима терапии при цистите в равной степени может быть связана как с антибактериальным препаратом, обеспечивающим своевременную и полноценную эрадикацию возбудителя, так и с иммунопрофилактикой, позволяющей восстанавливать местные и системные защитные механизмы с прицелом на иммунитет против основного возбудителя цистита – E. coli. Следует отметить, что исходя из различий между планируемым (n=250) и числом пациентов, включенных в исследование (n=52), экстраполяция данных в популяции ограничена.
Для больных, страдающих рецидивирующими инфекциями нижних мочевых путей, выбор антибактериального препарата должен основываться на результатах бактериологического исследования и анализа предшествующей антибиотикотерапии.
При обращении пациенток в период обострения цистита рекомендуется лечение полными курсовыми дозами антимикробных препаратов [7]:
- Фосфомицина трометамол 3 г одна доза каждые 10 дней в течение 3 мес или
- Фуразидина калиевая соль в сочетании с магния карбонатом основным по 100 мг 2 раза 7 дней, или
- Левофлоксацин по 500 мг 1 раз 5 дней, или
- Ципрофлоксацин по 500 мг 2 раза 5 дней, или
- Цефиксим 400 мг 1 раз в сутки 7 дней, или
- Цефтибутен 400 мг 1 раз в сутки 7 дней.
Цефиксим может быть одним из препаратов выбора с учетом региональных данных по определению чувствительности возбудителей рецидивирующих ИМП (ДАРМИС, 2010–2011) [6].
Итоги наблюдательной программы FLORA подтверждают эффективность комплексного подхода к терапии рецидивирующих ИМП препаратами Цефорал® Солютаб® и Уро-Ваксом® в условиях клинической практики врача-уролога.
Заключение. На основании данных, полученных в наблюдательной программе FLORA, можно утверждать, что схема лечения рецидивирующего цистита, включающая цефиксим по 400 мг 1 раз в день в течение 5–7 дней и Уро-Ваксом® по 1 капсуле 1 раз в день в течение 3 мес (одновременно с началом или после антибиотикотерапии) эффективна и хорошо переносима.
Исследование проведено при поддержке компании «Астеллас Фарма Юроп Б.В.».


