Введение. Вторая часть нашей работы касается наиболее технически сложной процедуры – правосторонней илеоуретеропластики. Как показал анализ литературы, трудности возникают при замещении правого мочеточника кишечным сегментом с расположением его в изоперистальтическом направлении [1–3]. Большинство авторов предостерегают, что при правосторонней изоперистальтической кишечной пластике мочеточника может возникать перекрут брыжейки трансплантата, что чревато нарушением его трофики, некрозом и отторжением. Вместе с тем они не дают по этому поводу конкретных рекомендаций, как надо поступать, и во всех ли случаях в зависимости от анатомо-физиологических особенностей (короткая или длинная брыжейка) так происходит. По-видимому, это объясняется малым числом наблюдений. Наиболее аргументированно данный вопрос освещен в работах [2–4], которые рекомендуют во всех случаях располагать илеотрансплантат изоперистальтически, приводя в общих чертах возможные технические решения.
 R. E. Abdel-Halim и соавт. [5], располагая довольно скромным опытом пяти илеоуретеропластик у пациентов с шистосомозом мочевыводящих путей, также упоминают о данной проблеме. Авторы обращают внимание на технические трудности, связанные с перекрутом брыжейки и нарушением трофики трансплантата при правосторонней илеоуретеропластике. Н. А. Лопаткин и соавт. [6], также основываясь на небольшом опыте кишечной реконструкции мочеточников, констатируют, что проблем с изоперистальтическим расположением илеотрансплантатов у них не было, но не сообщают, как это надо делать.
R. E. Abdel-Halim и соавт. [5], располагая довольно скромным опытом пяти илеоуретеропластик у пациентов с шистосомозом мочевыводящих путей, также упоминают о данной проблеме. Авторы обращают внимание на технические трудности, связанные с перекрутом брыжейки и нарушением трофики трансплантата при правосторонней илеоуретеропластике. Н. А. Лопаткин и соавт. [6], также основываясь на небольшом опыте кишечной реконструкции мочеточников, констатируют, что проблем с изоперистальтическим расположением илеотрансплантатов у них не было, но не сообщают, как это надо делать.
Детально не описывают и, понятно, не иллюстрируют, как расположить взятый кишечный сегмент по отношению к петлям тонкого и отделам толстого кишечника, чтобы выполнить илеоуретеропластику справа в изоперистальтическом варианте без нарушения питания трансплантата, и те немногие исследователи, которые на сегодняшний день обладают наибольшим опытом таких операций [7–10]. В связи с этим в нашей работе мы хотели бы остановиться на основных особенностях ее выполнения.
Материалы и методы. С 2001 по 2015 г. в клинике урологии СЗГМУ им. И. И. Мечникова изолированная пластика мочеточников участком подвздошной кишки проведена 78 больным. С учетом двусторонних пластик и удвоения мочевыводящих путей изолированным участком подвздошной кишки замещен 101 мочеточник. В 56 (55,4%) случаях оперирован левый мочеточник, в 45 (44,6%) – правый.
 Техника замещения правого мочеточника изоперистальтически расположенным кишечным участком.
Техника замещения правого мочеточника изоперистальтически расположенным кишечным участком.
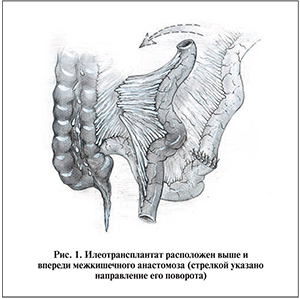
В зависимости от клинической ситуации выполняем срединную лапаратомию, люмболапаротомию, комбинированный доступ двумя разрезами, или используем лапараскопический доступ [11–13]. После ревизии брюшной полости берем сегмент подвздошной кишки необходимой длины и располагаем его в обязательном порядке выше и впереди межкишечного анастомоза. Помещение его ниже и позади межкишечного соустья, а затем поворот на 180˚ в изоперистальтическое положение в сторону лоханки правой почкой с большой долей вероятности приведет к перекруту брыжейки и некрозу трансплантата.
Выкраивание кишечного сегмента следует рассчитывать по поперечной длине его брыжейки. Она должна быть такой, чтобы без натяжения могла располагаться от оставшегося почечного конца мочеточника или лоханки до мочевого пузыря. При тотальной илеоуретеропластике участок кишки укорачиваем и выпрямляем по Ballivet, как это делаем при такой же операции слева. Затем его вместе с брыжейкой поворачиваем слева направо, словно перелистывая книжную страницу, тем самым осуществляя не винтообразный разворот кишечного трансплантата по оси в вертикальной плоскости с перекрутом брыжейки, а поворот на 160–180˚ в горизонтальной плоскости, не нарушая питания (рис. 1, 2). В результате трансплантат вместе с его брыжейкой, развернутые обратной стороной, ложатся в изоперистальтическом положении медиально от слепой и восходящей кишки параллельно мочеточнику. При этом межкишечный анастомоз подтягивается и становится расположенным слева от них. Такой технический прием без перекрута брыжейки нельзя осуществлять, если илеотрансплантат расположен ниже и позади межкишечного анастомоза.
Далее возможны два основных варианта продолжения операции. В первом мы оставляем этот взятый для пластики участок тонкой кишки в таком же положении, т.е. изоперистальтически медиально от восходящей ободочной кишки. Затем почечный конец мочеточника проводим через брыжейку восходящей толстой кишки в брюшную полость и осуществляем проксимальный уретероилеоанастомоз «конец в конец» или «конец в бок». Если сохранена только лоханка, то проксимальный конец трансплантата проводим через окно в брыжейке толстого кишечника в забрюшинное пространство и выполняем пиелоилеоанастомоз. Дистальный конец кишечного трансплантата проводим над терминальным отделом тонкого кишечника или через его брыжейку вниз к мочевому пузырю и осуществляем илеоцистоанастомоз (рис. 3). Все анастомозы накладываем на интубаторах или стентах с использованием викрила 3,0. Мочевой пузырь дренируем катетером Фолея, интубатор выводим вместе с ним по уретре.
Недостаток данного метода состоит в следующем: в своей дистальной части трансплантат пересекает сверху подвздошный отдел кишечника. Подобное расположение таит опасность непроходимости тонкого кишечника в результате вхождения его петель через образовавшееся большое округлое отверстие, границами которого по верхней полуокружности являются брыжейка трансплантата, сам трансплантат и мочевой пузырь, а по нижней – париетальная брюшина малого таза. Облитерировать его путем наложения швов между трансплантатом и париетальной брюшиной невозможно, так как там проходит терминальный отдел подвздошной кишки. Для того чтобы минимизировать риск подобного осложнения, мы делаем это пространство максимально широким, выполняя илеоцистоанастомоз в области дна мочевого пузыря.
Примером служит клиническое наблюдение, когда п а ц и е н т к е Б. 52 лет с постлучевой протяженной облитерацией правого мочеточника, гидроуретеронефрозом, нефростомой 05.06.01 выполнен изоперистальтический уретероилеоцистанастомоз справа. Осложнений после операции не наблюдалось. При контрольном обследовании через 2, 4 года и через 13 лет функция правой почки хорошая, нарушений уродинамики нет (рис. 4). При цистоскопии определяется хорошо проходимое артифициальное устье кишечного мочеточника (рис. 5).
По нашему мнению, хорошая функция почки и мочевыводящих путей с включенным в них участком кишки в отдаленном послеоперационном периоде в данном случае обусловлена изоперистальтическим расположением кишечного трансплантата.

Выполняя операцию во втором варианте, мы основываемся на технике, предложенной в 1957 г. R. Küss. Взятый и повернутый слева направо кишечный трансплантат через широкое отверстие в бессосудистой зоне брыжейки восходящей ободочной кишки переводим в пространство правого бокового канала и укладываем его латерально и позади слепой и восходящей ободочной кишки. В зависимости от степени обструкции осуществляем уретероилеоанастомоз (рис. 6, а) или пиелоилеоанастомоз (рис. 6, б), а затем в обход и ниже слепой кишки – илеоцистоанастомоз однорядным викриловым швом. Интубатор анастомоза вместе с катетером Фолея выводим по уретре и дренируем брюшную полость.
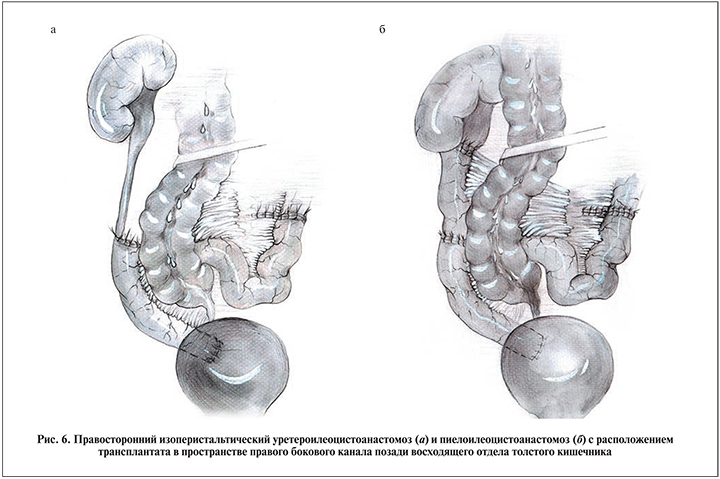
Таким образом, участок кишки, выполняющий функцию мочеточника, полностью находится внутрибрюшинно, располагаясь в правом боковом канале позади восходящей и слепой кишки в стороне от петель тонкого кишечника. К преимуществам данного метода, по нашему мнению, относятся, во-первых, то, что кишечный трансплантат располагается изоперистальтически, без перекрута его брыжейки. Во-вторых, он находится на всем протяжении в естественном для себя состоянии в брюшной полости, тесно прилегая к париетальной брюшине. В-третьих, такое его латеральное расположение в правом боковом канале без перекреста с основной кишечной трубкой исключает образование перемычек и пространств, в которых возможно сдавливание петель тонкого кишечника. В-четвертых, так можно заместить дефект правого мочеточника любой протяженности вплоть до тотальной илеоуретеропластики. Недостатком такого подхода является относительная сложность операции с необходимостью широкой мобилизации брыжейки трансплантата. Удлинение брыжейки осуществляем, во-первых, за счет более глубокого выделения ее по направлению к корню, во-вторых, – посредством резекции 5–7 см концов илеотрансплантата. Примером служит следующее наблюдение.
 П а ц и е н т к а Е. 39 лет госпитализирована в нашу клинику 19.06.14 в плановом порядке с жалобами на наличие нефростомы справа. Из анамнеза известно, что 04.03.14 поступила по поводу третьих срочных родов в один из роддомов Санкт-Петербурга, где проводилось клинико-лабораторное обследование и подготовка к оперативному родоразрешению. У больной имелись рубец на матке после двух операций кесарева сечения, отеки беременной, предлежание плаценты, полное прорастание плацентарной ткани в нижний сегмент и сосудистый пучок справа, синдром аортокавальной компрессии, варикозная болезнь вен нижних конечностей, анемия тяжелой степени.
П а ц и е н т к а Е. 39 лет госпитализирована в нашу клинику 19.06.14 в плановом порядке с жалобами на наличие нефростомы справа. Из анамнеза известно, что 04.03.14 поступила по поводу третьих срочных родов в один из роддомов Санкт-Петербурга, где проводилось клинико-лабораторное обследование и подготовка к оперативному родоразрешению. У больной имелись рубец на матке после двух операций кесарева сечения, отеки беременной, предлежание плаценты, полное прорастание плацентарной ткани в нижний сегмент и сосудистый пучок справа, синдром аортокавальной компрессии, варикозная болезнь вен нижних конечностей, анемия тяжелой степени.
19.03.14 в экстренном порядке в связи с массивным кровотечением была родоразрешена путем кесарева сечения. Учитывая продолжающееся кровотечение в связи с прорастанием плацентарной ткани в нижний сегмент и правый параметрий с поражением сосудистого пучка, объем операции был расширен до экстирпации матки без придатков с предварительной перевязкой внутренней подвздошной артерии справа при участии сосудистого хирурга. Общая кровопотеря – 6500 мл, выполнена аутогенная трансфузия в объеме 3000 мл.
Течение послеоперационного периода осложнилось кровотечением в брюшную полость и забрюшинное пространство, что потребовало 19.03.14 релапаротомии, двусторонней аднексэктомии, удаления гематомы забрюшинного пространства, дренирования брюшной полости, перевязки внутренней подвздошной артерии, ушивания повреждения внутренней подвздошной вены. Интраоперационная кровопотеря – 3700 мл. В послеоперационном периоде проводились реанимационные мероприятия: аутогемореинфузия, гемо- и плазмотрансфузия. Однако состояние больной не улучшалось. Появилась клиника мочевого перитонита в результате ишемии, некроза и перфорации стенки правого мочеточника в средней трети.
25.03.14 в экстренном порядке выполнены релапаротомия, ревизия брюшной полости и забрюшинного пространства, резекция правого мочеточника в средней трети с анастомозом «конец в конец» на стенте, интубация кишечника зондом Эббота, дренирование забрюшинного пространства и брюшной полости, трахеостомия. 05.04.14 проведена очередная экстренная операция по поводу несостоятельности межмочеточникового анастомоза, некроза мочеточника, мочевого затека и флегмоны забрюшинного пространства. Выполнены открытая нефростомия, удаление мочеточника, дренирование забрюшинного пространства. 25.04.14 трансректальное вскрытие и дренирование пресакрального абсцесса, после чего состояние больной стало улучшаться и 06.05.14 в удовлетворительном состоянии она была выписана на амбулаторное лечение с рекомендацией обратиться в нашу клинику. При поступлении на антеградной и ретроградной пиелоуретерографии определятся дефект мочеточника от лоханки до предпузырного отдела (рис. 7).
01.07.14 выполнена лапаротомия с обходом пупка слева. С техническими трудностями острым путем разделены петли тонкого кишечника, выделены из спаек слепая и восходящая ободочная кишка. Отступя 30 см от илеоцекального угла, резецирован сегмент подвздошной кишки длиной 50 см. Расстояние между концами его брыжейки составило 30 см. Взятый трансплантат повернут слева направо в изоперистальтическом положении. Излишки кишечных петель в его центральной части длиной 14 см резецированы по Ballivet с целью удлинения брыжейки, удален также избыточный дистальный конец трансплантата длиной 5 см. В бессосудистой зоне брыжейки восходящей ободочной кишки сформировано отверстие, через которое трансплантат проведен в область правого бокового канала. Выполнен илеоцистоанастомоз «конец в конец». Проксимальное отверстие кишечного трансплантата ушито и фиксировано викриловым швом к брюшине над правой почкой.
20.08.14 вновь поступила в клинику для второго этапа операции. Произведена люмботомия справа. Острым путем из рубцовых сращений под контролем введенного через свищевой ход бужа выделены почка, нижние и верхние сегментарные сосудистые пучки и между ними передняя поверхность лоханки. Почечная паренхима сохранена. Лоханка вскрыта разрезом длиной 1,5 см. Выделен латерально расположенный от восходящей кишки подготовленный для пластики тонкокишечный сегмент. Проксимальный конец его вскрыт. Выполнен передний лоханочно-кишечный анастомоз узловыми викриловыми швами на интубаторе, который выведен наружу вместе с нефростомой (рис. 8). Рана дренирована и послойно ушита. Послеоперационное течение гладкое. На антеградной пиелоилеограмме справа определяется хорошо проходимый до мочевого пузыря артифициальный мочеточник (рис. 9). Нефростома удалена, свищ закрылся. 09.09.14 больная в удовлетворительном состоянии выписана на амбулаторное лечение. Через 3 и 12 мес после операции проведена мультиспиральная компьютерная томография с контрастированием, по данным которой определен хорошо проходимый сформированный из подвздошной кишки правый мочеточник.
 В данном клиническом наблюдении приведена сложная многоэтапная реабилитация роженицы, первоначально находившейся в одном из лучших перинатальных центров Санкт-Петербурга, а на заключительных этапах – в нашей клинике. Окончательное выздоровление больной наступило после выполнения ей тотальной изоперистальтической илеоуретеропластики справа, позволившей устранить мочевой свищ и сохранить почку.
В данном клиническом наблюдении приведена сложная многоэтапная реабилитация роженицы, первоначально находившейся в одном из лучших перинатальных центров Санкт-Петербурга, а на заключительных этапах – в нашей клинике. Окончательное выздоровление больной наступило после выполнения ей тотальной изоперистальтической илеоуретеропластики справа, позволившей устранить мочевой свищ и сохранить почку.
Результаты. Период наблюдения составил от 3 мес до 14 лет (средний – 8,3±0,8 года). Всеми пациентами достигнуто восстановление уродинамики и нормализация функции почек. Среди 78 больных ранние послеоперационные осложнения возникли у 8 (10,2%) пациентов, 5 (6,4%) из которых потребовались повторные операции. В отдаленном послеоперационном периоде осложнения развились у 7 (8,9%) больных и четверым потребовалось оперативное лечение. У этих пациентов образовались стриктуры уретероилеоанастомозов спустя 3 мес и более после операции. Проходимость мочевыводящих путей была восстановлена путем антеградного бужирования стриктур. Результаты консервативного лечения и повторных операций для всех пациентов оказались хорошими. Летальных исходов не было.
Заключение. Правосторонняя, особенно тотальная, илеоуретеропластика – наиболее технически сложный из возможных вариантов замещения мочеточника кишечным участком. Чтобы выполнить ее в изоперистальтическом варианте без перекрута брыжейки илеотрансплантата, следует правильно расположить его по отношению к межкишечному анастомозу, а именно выше и кпереди от него. Лучшим из последующих продолжений операции является расположение трансплантата в правом боковом канале позади слепой и восходящей ободочной кишки.


