Введение. Открытая аденомэктомия считалась традиционным методом лечения при инфравезикальной обструкции, вызванной доброкачественной гиперплазией предстательной железы (ДГПЖ) объемом свыше 100 см3, обеспечивая положительные долгосрочные результаты [1–5]. M. Mariano и соавт. было показано, что эндовидеохирургическая (ЭВХ) аденомэктомия обеспечивает те же функциональные результаты, что и открытая аденомэктомия, обладая преимуществами в виде меньшей общей кровопотери, времени внутрипузырного орошения, длительности катетеризации и количества послеоперационных койко-дней [3].
В 1996 г. P.J. Gilling впервые была описана техника гольмиевой лазерной энуклеации предстательной железы (HoLEP), которая заключалась в анатомически обоснованном иссечении долей простаты до хирургической капсулы. В 1998 г. техника была доработана и дополнена авторами – после выделения и энуклеации доли смещали в ретроградном направлении в мочевой пузырь, где их в последующем подвергали морцелляции [4].
Гольмиевая лазерная энуклеация простаты имеет схожие результаты улучшения максимальной скорости потока мочи (Qmax) и баллов шкалы IPSS с низкой степенью послеоперационных осложнений в ряде длительных последующих наблюдений по сравнению с открытой аденомэктомией [5, 6]. Мета-анализ рандомизированных исследований показал, что по сравнению c традиционной аденомэктомией лазерная энуклеация также имела преимущества в виде значительного снижения кровопотери, длительности катетеризации и количества послеоперационных койко-дней [5].
Многоцентровый мета-анализ, опубликованный в 2010 г., позволил сделать заключение, согласно которому HoLEP является единственной эндоскопической процедурой с доказанной высокой эффективностью по сравнению с трансуретальной резекцией простаты (ТУРП) [7]. HoLEP получила широкое распространение как эндоурологическая альтернатива открытым аденомэктомиям в хирургическом лечении аденом больших объемов.
В настоящее время для лечения аденомы предстательной железы свыше 100 см3 в различных стационарах используются различные методы: открытые, эндоскопические и эндовидеохирургические.
Целью настоящего исследования было сравнить и оценить эффективность наименее инвазивных оперативных вмешательств в лечении: HoLEP с ЭВХ- аденомэктомией.
Материалы и методы. Исследование было одобрено этическим комитетом СПбГБУЗ «Клиническая больница Святителя Луки».
Пациенты. Проведено сравнение 90 ЭВХ-аденомэктомий и 90 HoLEP, выполненных при больших аденомах (более 100 см3). Были проанализированы данные, собранные от 180 пациентов, нуждающихся в хирургическом лечении в связи с выраженной гипертрофией аденоматозной ткани простаты по данным ультразвукового исследования. Наличие конкрементов мочевого пузыря являлось причиной исключения из исследования. Все операции были выполнены одним опытным хирургом на базе различных стационаров Российской Федерации в период с января 2015 по декабрь 2016 г.
Оперативные техники
Эндовидеохирургическая аденомэктомия
Вмешательства проводили из экстраперитонеального доступа с использованием 5 троакаров. Доступ для камеры (10 мм) был расположен справа от пупка, на 8 см латерально и книзу с обеих сторон под визуальным контролем устанавливали 2 порта: слева – 10 мм, справа – 5 мм. На среднем расстоянии по линии между правым и левым троакарами и лапароскопом устанавливали 2 троакара 5 мм. Перевязку боковых ножек простаты или дорсального комплекса не применяли. Поперечный разрез выполняли по передней поверхности простатической капсулы, используя аппарат ThunderBeat, совмещающий ультразвуковую и биполярную энергии. Считаем, эта техника обеспечивает лучшую визуализацию ткани предстательной железы, что позволяет выполнять более качественный гемостаз. Гемостаз капсулы осуществляли путем биполярной коагуляции. Проводили тригонизацию слизистой мочевого пузыря к слизистой уретры. Простатическую капсулу ушивали непрерывным швом (2:0 нить V-lock, игла 5/8). После ушивания устанавливали 3-ходовый профилированный катетер 18 Ch. Для проверки герметичности шва мочевой пузырь наполняли стерильным раствором 0,9% NaCl в объеме 200 мл. Важно отметить, что баллон катетера раздували после проверки герметичности шва, так как возможно получение ложных данных о целостности из-за блокирования дефекта поверхностью раздутого баллона катетера. Доли помещали в контейнер и извлекали. Во всех наблюдениях операцию завершали установкой дренажа из поливинилхлорида (ПВХ) в зону операции.
Гольмиевая лазерная энуклеация простаты
Использовали гольмиевый лазер с длиной волны 2140 нм (Versapulse+Lumenis, 100W). Основным инструментом служил специальный лазерный резектоскоп с ирригацией физиологическим раствором диаметром 26 Fr, адаптированный для многоразового волоконного лазера. После цистоскопии и идентификации устьев мочеточника выполняли энуклеацию. Первоначально лазером отмечали три линии на 5, 7 и 12 ч условного циферблата. Для удаления средней доли создавали полость между позициями на 5 и 7 ч от шейки мочевого пузыря до семенного бугорка. Эта полость была далее распространена кзади до простатической капсулы и таким образом среднюю долю энуклеировали и помещали в мочевой пузырь [8]. Аналогичным способом удаляли каждую долю: лазером воздействовали на пространство между аденомой и простатической капсулой ретроградно от семенного бугорка до шейки мочевого пузыря. Эту энуклеационную поверхность обрабатывали лазером до тех пор, пока аденома не отсоединялась и не погружалась в мочевой пузырь. Для гемостаза использовали энергию гольмиевого лазера. После энуклеации долей аденоматозную ткань измельчали и удаляли трансуретрально, используя морцелляционный эндоскоп 5 мм (morce-scope Olympus). В конце операции устанавливали 3-ходовый профилированный уретральный катетер диаметром 20–22 Fr.
Статистический анализ
Пациенты в двух группах были попарно соотнесены согласно качественным (возраст, ASA-группа) и параметрическим (объем простаты по данным УЗИ) критериям. Результаты пред- и послеоперационных данных (через 3 мес.) по шкале IPSS и максимальной скорости потока мочи были оценены с помощью t-критерия Стьюдента. Оценивали объем простаты по данным ультразвукового исследования: время операции, длительность катетеризации, продолжительность послеоперационной ирригации мочевого пузыря, необходимость трансфузии и длительность послеоперационного койко-дня. Частоту послеоперационных осложнений оценивали, согласно модифицированной классификации хирургических осложнений, тестом точности Фишера.
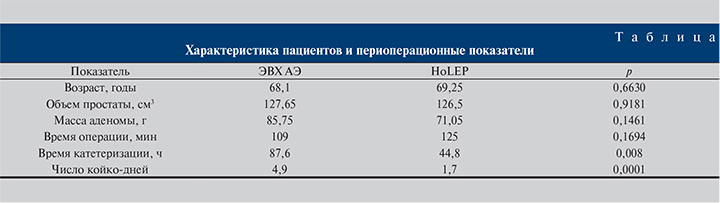
Результаты. Группы были сопоставимыми по возрасту пациентов и исходному объему простаты по данным УЗИ. Продолжительность катетеризации и пребывания в клинике в группе HoLEP была статистически значимо ниже (см. таблицу).
Гистопатологическое исследование обнаружило доброкачественную гиперплазию простаты у всех пациентов, подвергшихся оперативному лечению.
В группе HoLEP средний балл по шкале IPSS снизился с 21 до 4,8 за 3 мес., прошедших с момента операции (р<0,0001), а Qmax выросла с 6,45 до 24,75 мл/с (р=0,0007). В группе ЭВХ АЭ соответствующие показатели составили 23,5 и 7,65 (р<0,0001), 8,95 и 24,81 мл/с (р<0,0001).
Разница между группами в показателях по шкале IPSS спустя 3 мес. оказалась статистически значимой (р=0,0103), тогда как по максимальной скорости потока мочи – нет.
Осложнения. В группе HoLEP осложнения возникли у 18 (20%) пациентов. В 17 наблюдениях они соответствовали 1-й степени по Clavien: у 12 человек была лихорадка в первый послеоперационный день, у 3 – острая задержка мочи после удаления катетера, у 2 – острая задержка мочи вследствие тампонады мочевого пузыря (купировалась консервативно). Только одному пациенту пришлось делать промывание мочевого пузыря сразу в день операции из-за выраженной гематурии (степень 3b).
В группе ЭВХ-аденомэктомии осложнения диагностировали у 23 (25,6%) пациентов. Двадцать из них – 1-й степени: у восьми была лихорадка, у девяти – гематурия, у пяти – острая задержка мочи вследствие тампонады мочевого пузыря, а у одного пациента осложнение 2-й степени – инфекция мочевыводящих путей с признаками бактериемии. Статистически значимой разницы в частоте осложнений между группами выявлено не было (р>0,99).
Обсуждение. В Европе и России открытая аденомэктомия была превалирующей хирургической процедурой, используемой при больших (>100 см3) размерах предстательной железы [2, 4, 9]. В настоящее время доля подобных вмешательств среди инвазивных процедур, используемых при ДГПЖ, составляет 14–32% [10]. Однако у этой техники существует ряд недостатков – время катетеризации, длительность пребывания в стационаре, необходимость в трансфузии, потребность в продолжительной катетеризации, длительное пребывание в стационаре, необходимость в трансфузии [11]. Все это послужило толчком к внедрению менее инвазивных хирургических методик для лечения ДГПЖ большого объема. Существует ряд минимально инвазивных хирургических вмешательств, которые проводятся в современной урологии, наиболее часто выполняемыми из которых являются биполярная ТУРП [12], лазерная энуклеация простаты [13–15], ЭВХ-аденомэктомия [2, 3, 10, 16–18].
Проведен ряд работ, посвященных сравнению различных минимально инвазивных хирургических вмешательств, однако на сегодняшний день очень мало работ по сравнению лазерной энуклеации и лапароскопической аденомэктомии. В настоящем исследовании мы сравнили HoLEP и ЭВХ-аденомэктомию, оценили их результаты, эффективность и безопасность.
В центрах с большим опытом проведения лапароскопических операций ЭВХ-аденмэктомия является признанной альтернативой малоинвазивной технике для лечения больших ДГПЖ. Данное оперативное пособие может рассматриваться для пациентов, которым противопоказаны трансуретральные процедуры (стриктуры уретры, предшествующая уретропластика, ортопедическая патология), или пациентов с ДГПЖ на фоне больших дивертикулов мочевого пузыря или больших камней. Сравнительный анализ показал, что результатом эндовидеохирургических вмешательств по сравнению с открытой аденомэктомией является меньший объем кровопотери, сокращение сроков катетеризации/ирригации и пребывания в стационаре при сопоставимых функциональных результатах (балл IPSS, Qmax) [2, 17].
Лазерная энуклеация завоевала широкую популярность как малоинвазивная альтернатива открытой аденомэктомии для лечения больших ДГПЖ. Три основных источника энергии, используемые для лазерной энуклеации, – это гольмий, туллий и калий-титанил-фосфат (КТР). Среди них HoLEP был выделен в положительную сторону благодаря массе использования в международной практике с превосходными функциональными результатами, эффективностью и безопасностью [5, 13, 15, 19]. В текущих европейских рекомендациях она рекомендована как главная альтернатива открытой аденомэктомии [9]. Ранее было описано, что кривая обучения для проведения HoLEP составляет более 50 процедур [20].
Лазерное лечение ДГПЖ – пока не «золотой» стандарт, однако его уже выбирают большинство пациентов с симптомной ДГПЖ. Кроме того, авторитетные ученые мирового уровня еще в 2013 г. предложили рассматривать трансуретральную HoLEP как новый «золотой» стандарт хирургического лечения ДГПЖ независимо от ее размеров [21].
Наше исследование продемонстрировало, что обе техники были высокоэффективными в лечении обструктивных симптомов. Тем не менее продолжительность катетеризации, пребывание в стационаре и балл по шкале IPSS спустя 3 мес. после операции свидетельствовали в пользу HoLEP. Интересно, что скорость потока мочи статистически значимо не различалась, а значит, разница в оценке по шкале IPSS скорее всего обусловлена раздражающими симптомами, связанными с техникой ЭВХ-аденомэктомии. Не было значимых различий между степенью осложнений по системе Клавиена между двумя группами.
Гольмиевую лазерную энуклеацию отличают более короткий срок пребывания в клинике, меньшая продолжительность катетеризации и превосходные функциональные результаты. Основные ограничения этой техники заключались в недостаточной морцелляции, потенциальной инфекции мочевого пузыря, связанной с морцеллятором и неполной морцелляцией. Тем не менее мы не столкнулись с какими-либо осложнениями, вызванными непосредственным воздействием морцеллятора.
Ограничениями нашего исследования стали относительно небольшое количество пациентов в каждой группе и отсутствие рандомизации. Однако уникальность исследования состоит в том, что мы оценили два минимально инвазивных подхода для больших (>100 см3) ДГПЖ в сравниваемых популяциях, выполняемых одним хирургом.
Заключение. В настоящее время использование сравниваемых методик одинаково обосновано для лечения аденомы предстательной железы свыше 100 см3.
HoLEP несет схожие краткосрочные функциональные результаты и осложнения по сравнению с ЭВХ АЭ при больших объемах ДГПЖ, но имеет преимущества во времени катетеризации, сокращенном пребывании в стационаре. Однако следует учесть, что данные послеоперационные результаты достигаются при проведении оперативного вмешательства опытным хирургом.


