Введение. Дистанционная литотрипсия (ДЛТ) является малоинвазивным методом лечения больных мочекаменной болезнью (МКБ) [1, 2]. Установлена зависимость эффективности лечения МКБ от денситометрической плотности, локализации, размеров, физико-химического состава мочевых камней, а также анатомо-функциональных особенностей строения почки [3–8]. С развитием медицинской техники появилась возможность определения упругости тканей с помощью нового ультразвукового метода – эластографии [7, 8]. Упругость – это свойство тел изменять форму и размеры под действием нагрузок и самопроизвольно восстанавливать исходную конфигурацию при прекращении внешних воздействий [9–11]. Другим важным показателем является физико-химическая структура мочевого камня, от которой зависит эффективность ДЛТ [12–15].
С помощью эластографии возможна количественная и качественная оценка ткани исследуемого органа [11–17]. В ранее проведенных исследованиях также определены параметры акустического сопротивления и динамического модуля упругости почечных камней [18–21]. Как указывают авторы, после оперативного удаления для проведения исследования мочевые камни помещались в фантом – искусственно смоделированные синтетические ткани почки. В зависимости от структуры и состава определены значительные вариации упругости камней в почках. При этом Е. Esch и соавт. (2010) экспериментальным путем установили диапазон различий ультразвуковых параметров – от 1816 по 3010 м/с – в зависимости от физико-химического состава мочевого камня. Камни, имеющие высокое содержание оксалата кальция, характеризуются наибольшей скоростью распространения ультразвуковой волны [20]. В свою очередь мочевые камни, имеющие больший процент фосфатов, показали наименьшую скорость распространения УЗ-волны. А. Gregory и соавт. (2015) на искусственной модели (фантоме) исследовали упругость сходных по физико-химическому составу (оксалат кальция) камней почки в зависимости от их размера. Минимальный размер мочевого камня в данном исследовании составил 2,0 мм и имел наименьшую упругость, соответственно Еmin – 20,9кПа. Максимальный размер составил мочевой камень 15 мм и имел наибольшую упругость до Emax – 213,50 кПа [21].

Цель исследования: изучить упругость мочевых камней для оценки физико-химического состава мочевого камня.
Материалы и методы. В клинике урологии ФГБОУ ВО «Первый МГМУ им. И. М. Сеченова» с октября по декабрь 2015 г. проведено исследование с участием 30 пациентов с мочекаменной болезнью (12 женщин и 18 мужчин) в возрасте от 25 до 65 лет (табл. 1).
Наибольшее количество пациентов мужского и женского пола было в возрасте от 45 до 55 лет – 7 (23,3%) и 5 (16,7%) пациентов соответственно. Пациентам проведено комплексное клиническое обследование с использованием лучевых методов (УЗИ, в/в урография, мультиспиральная компьютерная томография [МСКТ]) диагностики. Распределение пациентов по локализации и размерам камней представлено в табл. 2–3.
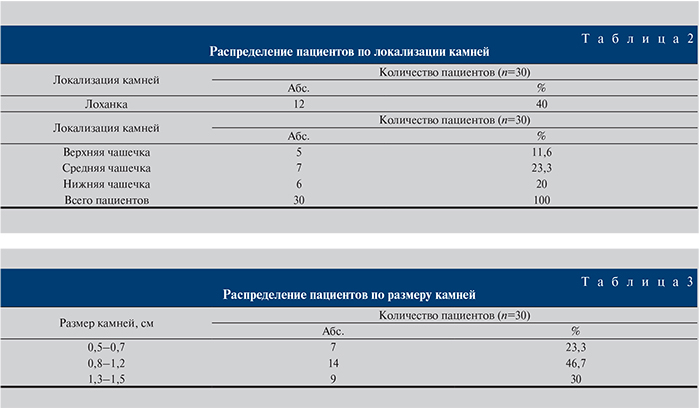
У 12 (40%) пациентов камни локализовались в лоханке: у 5 (11,6%) – в верхней, у 7 (23,3%) – в средней и у 6 (20%) – в нижней чашечках. Размер камней варьировался от 5 до 15 мм.
У 14 (46,6%) размер камней составил от 0,8 до 1,2 см, у 7 (23,3%) от 0,5 до 0,7, а у 9 пациентов от 1,3 до 1,5 см.
 Всем пациентам перед ДЛТ проводили определение степени упругости конкремента с помощью ультразвуковой эластографии сдвиговой волны (УЗЭСВ). Исследование осуществляли с помощью ультразвукового аппарата «Aixplorer» фирмы «SuperSonic Imagine S.A» (Германия) в режиме эластографии. Техника проведения эластографии аналогична стандартному исследованию УЗИ почек. При эластографии сдвиговых волн на разной глубине с определенной временной задержкой одна за другой создаются сфокусированные точки максимального давления, в результате чего сдвиговые волны формируют фронт в виде так называемого конуса Маха. Поперечные волны генерируются в теле человека. Распространение поперечных волн коррелирует с упругостью исследуемых тканей. Участки с различной скоростью сдвиговых волн кодируются разными цветами по шкале с определенным количеством цветовых ячеек, что дает возможность визуально выявлять зоны с разной эластичностью. В результате исследования формируется двухмерное цветовое изображение упругости тканей интересующей области – цветовая эластограмма сдвиговой волны. Кроме цветовой градации упругости параллельно выводятся цифровые значения упругости ткани, соответствующие цветовому спектру. С помощью фокуса наведения (Q-box) в области исследования определяются структуры с целью количественной оценки ткани органа, при этом каждый фокус имеет свой радиус исследования и в его пределах определяется цифровое значение упругости (Е) исследуемой структуры. Ультразвуковой датчик устанавливали на поясничную область в проекции почек. После получения на экране данных эластографии определяли зону интереса – место локализации мочевого камня. Путем наведения фокуса (Q-box) измеряли упругость мочевого камня в (кПа). С учетом характеристик УЗЭСВ в автоматическом режиме указываются интервалы максимальной и минимальной (Еmin–Emax), а также средней упругости (Emean) исследуемой ткани.
Всем пациентам перед ДЛТ проводили определение степени упругости конкремента с помощью ультразвуковой эластографии сдвиговой волны (УЗЭСВ). Исследование осуществляли с помощью ультразвукового аппарата «Aixplorer» фирмы «SuperSonic Imagine S.A» (Германия) в режиме эластографии. Техника проведения эластографии аналогична стандартному исследованию УЗИ почек. При эластографии сдвиговых волн на разной глубине с определенной временной задержкой одна за другой создаются сфокусированные точки максимального давления, в результате чего сдвиговые волны формируют фронт в виде так называемого конуса Маха. Поперечные волны генерируются в теле человека. Распространение поперечных волн коррелирует с упругостью исследуемых тканей. Участки с различной скоростью сдвиговых волн кодируются разными цветами по шкале с определенным количеством цветовых ячеек, что дает возможность визуально выявлять зоны с разной эластичностью. В результате исследования формируется двухмерное цветовое изображение упругости тканей интересующей области – цветовая эластограмма сдвиговой волны. Кроме цветовой градации упругости параллельно выводятся цифровые значения упругости ткани, соответствующие цветовому спектру. С помощью фокуса наведения (Q-box) в области исследования определяются структуры с целью количественной оценки ткани органа, при этом каждый фокус имеет свой радиус исследования и в его пределах определяется цифровое значение упругости (Е) исследуемой структуры. Ультразвуковой датчик устанавливали на поясничную область в проекции почек. После получения на экране данных эластографии определяли зону интереса – место локализации мочевого камня. Путем наведения фокуса (Q-box) измеряли упругость мочевого камня в (кПа). С учетом характеристик УЗЭСВ в автоматическом режиме указываются интервалы максимальной и минимальной (Еmin–Emax), а также средней упругости (Emean) исследуемой ткани.
Дистанционную нефролитотрипсию проводили на литотрипторе «Dornier Gemini» (Германия). После самостоятельного отхождения фрагментов мочевых камней определяли физико-химический состав конкремента с помощью рентгенофазового анализа.

Результаты и обсуждение. Для определения чувствительности и специфичности УЗЭСВ полученные данные сопоставили с результатами компьютерной денситометрии у обследованных пациентов (табл. 4).
Самое высокое среднее значение упругости (Emean) отмечено у моногидрата оксалата кальция – 39,8 кПа, самое низкое – у мочевой кислоты (14,6 кПа). Для двухфазного мочевого камня (вевеллит+гидроксилапатит) Emean составило 28,5 кПа. Самый высокий интервал значений упругости (Еmin–Emax) отмечен у моногидрата оксалата кальция – 23,2–55,7 кПа соответственно, а самый низкий – у мочевой кислоты (Еmin –Emax) 5,8–25,5 кПа.
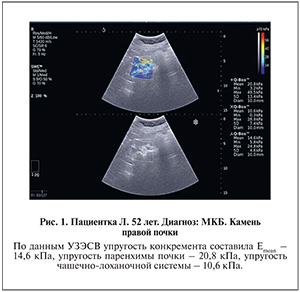
 Клиническое наблюдение 1. Пациентка Л. 52 лет. По данным ультразвукового исследования (УЗИ), компьютерной томографии (КТ) почек, выявлен камень правой почки размером 10х9 мм (рис. 1). Плотность мочевого камня составила 660 HU, упругость (Emean) – 14,6 кПа. Проведено оперативное лечение: ДЛТ камня правой почки. На фоне литокинетической терапии в послеоперационном периоде отмечено самостоятельное отхождение фрагментов мочевого камня на 5-е сутки после ДЛТ. Физико-химическая структура мочевого камня-урат (100%-ная мочевая кислота).
Клиническое наблюдение 1. Пациентка Л. 52 лет. По данным ультразвукового исследования (УЗИ), компьютерной томографии (КТ) почек, выявлен камень правой почки размером 10х9 мм (рис. 1). Плотность мочевого камня составила 660 HU, упругость (Emean) – 14,6 кПа. Проведено оперативное лечение: ДЛТ камня правой почки. На фоне литокинетической терапии в послеоперационном периоде отмечено самостоятельное отхождение фрагментов мочевого камня на 5-е сутки после ДЛТ. Физико-химическая структура мочевого камня-урат (100%-ная мочевая кислота).
Клиническое наблюдение 2. П а ц и е н т М. 41 года. По данным КТ, УЗИ почек выявлен камень нижней группы чашечек левой почки размером до 8х11 мм. Плотность мочевого камня – 1,400 HU, упругость (Emean) – 39,8 кПа. Проведено оперативное лечение: ДЛТ камня левой почки. Самостоятельное отхождение фрагментов мочевого камня на фоне литокинетической терапии отмечено на 4-е сутки после ДЛТ. Физико-химическая структура камня – моногидрат оксалата кальция (вевеллит) (рис. 2).
В исследованиях Е. Esch и соавт. (2010) и А. Gregory и соавт. (2015) УЗЭСВ мочевых камней проводилось на фантоме (искусственно смоделированные ткани почки) [20, 21]. Размер доступных исследованию мочевых камней составил от 2,0 до 15,0 мм. В нашем исследовании размер мочевых камней, доступных исследованию (эластография), составил от 5 до 15 мм.
Мочевые камни размером менее 5 мм не выделялись четким цветовым спектром в области исследования. В результате проведенного анализа нами определены средние показатели упругости, характерные для каждого отдельного вида мочевых камней (вевеллит: среднее значение плотности (Emean) – 39,8 кПа; мочевая кислота: среднее значение плотности (Emean) – 14,6 кПа.). Кроме того, мы сопоставили значения средней упругости и плотности мочевых камней различного физико-химического состава, данные представлены в табл. 4 (например: вевеллит: среднее значение плотности [Emean] – 1400 НU, среднее значение упругости [Emean] – 39,8 кПа). Однако считаем, что применение метода УЗЭСВ для прогнозирования физико-химического состава мочевого камня уступает по информативности физико-химическим методам и компьютерной денситометрии (МСКТ). Фактором, ограничивающим чувствительность УЗЭСВ, является превышение индекса массы тела, определяющего увеличение расстояния между ультразвуковым датчиком и мочевым камнем более 10 см, что значительно снижает информативность данного метода, так как пороговое расстояние генерации сдвиговой волны не превышает 10 см.
Заключение
- Эластография – метод, позволяющий определить степень упругости мочевых камней, измеряемый в кПа. Наибольшую среднюю упругость (Emean) по данным УЗЭСВ имели камни моногидрата оксалата кальция (вевеллит) (Emean) – 39,8 кПа, наименьшую – камни мочевой кислоты (Emean) – 14,6 кПа.
- Данные эластографии мочевых камней сопоставимы с результатами данными компьютерной денситометрии, так как средние показатели упругости и плотности имеют характерные значения для каждого отдельного вида мочевых камней.



